题目内容
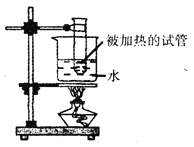
【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
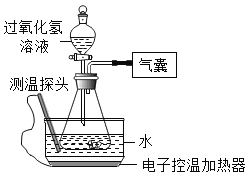
(猜想与假设)
影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂用量。
(实验记录)
同学们进行6组实验,实验记录如下:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的 浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的 体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | 0.1g MnO2 | 0.5g MnO2 | ||||
6min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是________mL。
(2)实验①-⑥可以通过测定__________来比较过氧化氢的分解速率。
A 相同时间内产生氧气的体积
B 产生相同体积的氧气所需时间
C 相同时间内产生氧气的质量
(3)得出“过氧化氢溶液的浓度越大分解速率越快”结论所依据的实验是____(填序号)。
(4)通过实验①、②、④可得出的结论是_________。
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是________(答一点即可)
【答案】6 AB ③④ 在相同条件下,温度越高,过氧化氢分解速率越大 实验②产生氧气少(或速率太慢或水蒸气含量高)
【解析】
(1)由于实验研究影响过氧化氢分解速率的因素温度、溶液的浓度、催化剂种类。所以要保证过氧化氢溶液的体积相同,所以x=6;
(2)氧气的密度较小的测量其质量不方便,比较过氧化氢的分解速率可通过相同时间内产生氧气的体积或产生相同体积的氧气所需的时间,进行比较。故选AB;
(3)过氧化氢溶液的浓度越大分解速率越大,所以实验的变量为:过氧化氢溶液的浓度,所以可通过③④进行对比;
(4)①、②、④的变量为水槽中水的温度,通过实验①、②、④可得出的结论是在相同条件下,温度越高,过氧化氢分解速率越大;
(5)相同时间内实验②产生氧气少,速率太慢并且由于水温过高,水蒸气含量高。

 名校课堂系列答案
名校课堂系列答案