题目内容
【题目】实验室有碳酸钡和碳酸钙的固体混合物50g,与足量盐酸充分反应,将反应后的溶液蒸干得到53.3g固体,则原混合物中金属元素的质量分数为( )
A. 64%B. 40%C. 36%D. 69.5%
【答案】A
【解析】
碳酸钡、碳酸钙与稀盐酸反应的化学方程式分别为BaCO3+2HCl═BaCl2+H2O+CO2↑、CaCO3+2HCl═CaCl2+H2O+CO2↑,由上述化学方程式可知,碳酸钡、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相对原子质量的和是71,一个碳酸根的相对原子质量是60,差是11,即完全反应后质量增加了11份质量。实际反应后固体质量增加了53.3g﹣50g=3.3g,设原混合物中含碳酸根的质量为x,则60:11=x:3.3g,x=18g,则所含金属元素质量为50g﹣18g=32g,原混合物中金属元素的质量分数为![]() ×100%=64%,故选A。
×100%=64%,故选A。

【题目】某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
(1)甲同学实验操作如下:
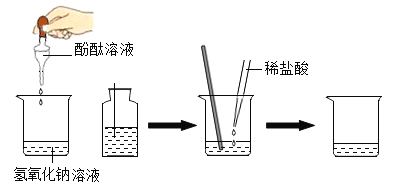
在烧杯中加入约5 mL氢氧化钠溶液、滴入几滴无色酚酞溶液,此时溶液呈________色。接着用滴管滴入一定量的稀盐酸,再用玻璃棒____________,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为________________________。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
(实验探究)反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:NaCl和HCl
猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是________________。
为了验证另外两种猜想,乙同学设计如下实验方案。
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | ________ | 猜想二成立 |
(反思交流)实验结束后,废液处理方法正确的是______(填序号)。
A 倒入下水道 B 倒入废液缸 C 带出实验室
(拓展延伸)乙同学再设计一个验证猜想二的实验:取少量反应后的溶液于试管中加入少量氧化铜粉末,若________________________,猜想二成立。
(3)用溶质质量分数为5%的NaOH溶液完全中和73 g10%的稀盐酸,需NaOH溶液多少克________?