题目内容
【题目】据报道,“火星快车”号探测器在火星大气层中发现一种二氧化碳分子,它的化学式为:![]() (元素符号左上角的数字代表该原子中的质子数和中子数之和).
(元素符号左上角的数字代表该原子中的质子数和中子数之和).
(1)![]() 中的质子数是_______;中子数是_______;
中的质子数是_______;中子数是_______;
(2)相同分子个数的![]() 和
和![]() ,所含氧元素的质量:前者_______后者(选填“大于”、“小于”或“等于”).
,所含氧元素的质量:前者_______后者(选填“大于”、“小于”或“等于”).
【答案】8 10 小于
【解析】
(1)16O和18O属于同种元素的原子,具有相同的电子数和质子数,原子核内的中子数和相对原子质量不同,故18O中的质子数是8;中子数=相对原子质量﹣质子数=18﹣8=10;
(2)C16O2的相对分子质量为12+16×2=44,C16O18O的相对分子质量=12+16+18=46,故由于每个分子中碳元素的质量相同,相同分子个数的两种物质中前者小于后者。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】下表是元素周期表中第2、3周期的元素,请回答有关问题。
2 | 3 锂 6.941 | 4 铍 9.012 | 5 硼 10.81 | 6 碳 12.01 | 7 氮 14.01 | 8 氧 16.00 | 9 氟 19.00 | 10 氖 20.18 |
3 | 11 钠 22.99 | 12 镁 24.31 | 13 铝 26.98 | 14 硅 28.09 | 15 磷 30.97 | 16 硫 32.06 | 17 氯 35.45 | 18 氩 39.95 |
(1)铝元素的相对原子质量为________________;
(2)下列各组具有相似化学性质的元素是_______________(填字母序号);
A![]() B
B![]() C
C![]() D
D![]()
(3)第8号元素与第13号元素的原子形成化合物的化学式为_______________;
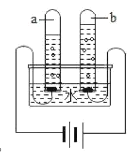
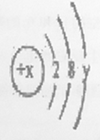
(4)某粒子的结构如图,当![]() 时,该粒子的符号为_______________;
时,该粒子的符号为_______________;
【题目】有一黑紫色的固体为KnMO4和MnO2的混合物,为测定混合物中KMnO4的质量,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 34.2 | 33.4 | 32.6 | 31.8 | 31.8 |
分析表中数据,完成下列问题:
(1)反应到___________min时反应完毕;
(2)该样品中KMnO4的质量_______。