题目内容
【题目】根据下图回答有关问题:

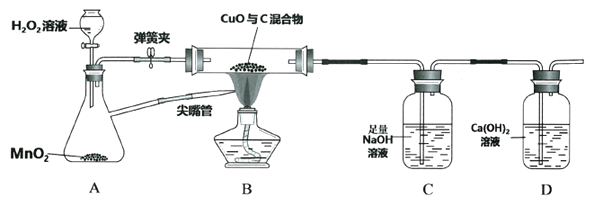
(1)写出实验①中反应的化学方程式________
(2)实验②可证明铁的金属活动性比铜强,因为能观察到液面下铁片的表面上会___(填写观察到的现象)。
(3)实验③中可观察到试管中铁钉最先生锈的是_________处。(填“a”或“b”或“c”)
【答案】 3Fe+2O2![]() Fe3O4 附着一层红色的固体 b
Fe3O4 附着一层红色的固体 b
【解析】(1)铁和氧气在点燃条件下生成四氧化三铁,反应的化学方程式3Fe+2O2![]() Fe3O4 ;(2)活动性强的金属能将活动性弱的金属从盐溶液中置换出来。实验②能观察到液面下铁片的表面上会红色固体,说明铁和硫酸铜反应 置换出溶液中的铜,可证明铁的金属活动性比铜强;(3) 铁生锈是铁与氧气、水共同作用的结果,实验③中可观察到试管中铁钉最先生锈的是b处,因此处铁与氧气、水接触最充分。
Fe3O4 ;(2)活动性强的金属能将活动性弱的金属从盐溶液中置换出来。实验②能观察到液面下铁片的表面上会红色固体,说明铁和硫酸铜反应 置换出溶液中的铜,可证明铁的金属活动性比铜强;(3) 铁生锈是铁与氧气、水共同作用的结果,实验③中可观察到试管中铁钉最先生锈的是b处,因此处铁与氧气、水接触最充分。

 阅读快车系列答案
阅读快车系列答案【题目】下列事实解释不正确的是()
选项 | 事实 | 解释 |
A | NaOH 和 |
|
B | 金刚石、石墨高温下都可以燃烧 | 它们都是有碳原子构成的 |
C | 给装满水的纸杯加热,开始时纸杯完好无损 | 温度没有达到纸的着火点 |
D | 酒精灯不用时,需用灯帽盖好 | 防止酒精挥发到空气中 |
A. A B. B C. C D. D
【题目】下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g 水)。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
①20℃时溶解度较大的物质是_________ ;
②除去KNO3晶体中混有的少量 NaCl,通过溶解、蒸发浓缩、______、过滤、洗涤、干燥得到比较纯净的KNO3晶体。滤液中溶质的成分有___________。
③用 4 只小烧杯取 T℃时的水各 50 克,进行实验并记录数据如下:
实验编号 | 1 | 2 | 3 | 4 |
KNO3 质量/g | 40 | 50 | 60 | 70 |
H2O质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 90 | 100 | 105 | X |
Ⅰ.实验 1 所得溶液的质量分数为_______ ,实验 4 中 X 的值为 _________,
Ⅱ. T℃时KNO3 的溶解度是 _________ g/100g 水。