题目内容
将氢氧化钠和氯化钠的混合物19.3g,放入80.7g水中使其完全溶解,再加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应.试计算:
(1)l00g 7.3%的稀盐酸中溶质的质量.
(2)原混合物中氢氧化钠的质量.
(3)反应后所得溶液中溶质的质量分数.
(1)7.3g (2)8g (3)11.5%
解析试题分析:(l)稀盐酸中溶质的质量为:l00g×7.3%=7.3g;
(2)设氢氧化钠的质量为x,生成氯化钠的质量为y.
NaOH+HCl=NaCl+H2O
40 36.5 58.5
X 7.3g y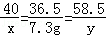
解得:x=8g y=11.7g
(3)所得溶液中溶质的质量分数为: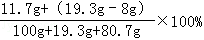 =11.5%
=11.5%
答:(1)l00g 7.3%的稀盐酸中溶质的质量是7.3g;
(2)原混合物中氢氧化钠的质量是8g;
(3)反应后所得溶液中溶质的质量分数是11.5%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:本题考查学生利用酸碱发生的化学反应方程式来进行的有关计算,学生应明确反应后的溶液中的溶液中溶质的来自两部分,利用质量守恒定律会计算溶液的总质量是解答此类习题的关键.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。
确定某种气体的实验室制法时,不需要考虑的是 ( )
| A.反应所需药品和反应条件 | B.实验装置 |
| C.气体的验证 | D.气体的用途 |