题目内容
【题目】向足量稀硫酸溶液中加入锌粉(仅含不溶于酸的杂质),充分反应,反应前后各物质的质量统计如图所示。求:
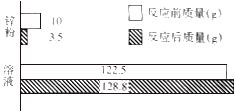
(1)锌粉中含有金属锌的质量为_____g。
(2)反应后,溶液中硫酸锌的质量分数为多少__________?(请写出计算过程)
【答案】 6.5g 12.5%
【解析】根据质量守恒定律和题中信息,生成氢气质量是122.5g+10g-128.8g-3.5g=0.2g。(1)锌粉中含有金属锌的质量为10g-3.5g=6.5g。
(2)解:设反应后,溶液中硫酸锌的质量分数为x
Zn+H2SO4 =ZnSO4+H2↑
161 2
128.8g×x 0.2g
![]() =
=![]() ,x=12.5%。
,x=12.5%。
答∶(1)锌粉中含有金属锌的质量为6.5g。(2)反应后,溶液中硫酸锌的质量分数为12.5%。
点睛∶灵活应用质量守恒定律,并正确书写化学方程式是顺利完成本题的重要保证。

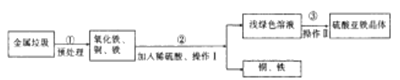
【题目】氧化铜矿石含有CuO、Cu2(OH)2CO3和Fe2O3,还含有一些不溶于水、不溶于酸的其他杂质。铜、铁是畜禽所必需的微量元素,某饲料厂联合生产硫酸铜晶体和硫酸亚铁晶体的主要工艺流程如下。
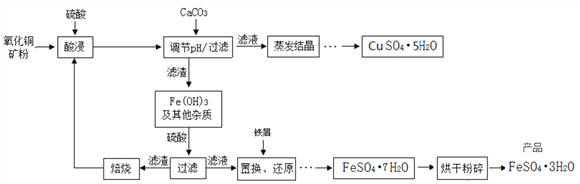
【资料】Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 |
开始沉淀的pH | 1.5 | 4.2 |
沉淀完全的pH | 3.7 | 6.7 |
请回答问题:
(1)氧化铜矿石粉碎的目的是________________________________。
(2)写出“酸浸”中发生反应的化学方程式__________________(任写一个)。
(3)该流程中氢氧化铁能与硫酸反应,其基本反应类型是_________反应。
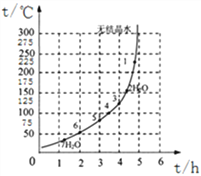
(4)下图为“硫酸亚铁干燥曲线图”,据此可确定由FeSO4·7H2O脱水得到流程中所示产品的适宜工艺条件为__________________(填写温度和时间)。
(5)在“调节pH/过滤”中,加入CaCO3调节溶液的pH,请说出溶液适宜的pH范围是____________。