题目内容
【题目】现有一包粉末,已知它们可能由Na2SO4、CuCl2、Na2CO3、KNO3中的一种或几种组成,某学生的实验过程记录如下:
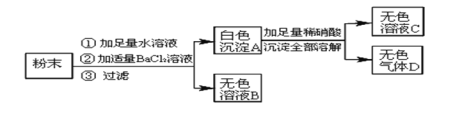
(1)KNO3 ___________(“是”或者“不是”)复合肥。
(2)白色沉淀A的化学式为_________,无色气体D的名称为__________。
(3)无色溶液B中一定含有的溶质是_________,可能含有的溶质是_____________。
(4)由上述实验记录推断:原粉末中一定不含_________________。
【答案】 是 BaCO3 二氧化碳 NaCl KNO3 CuCl2、Na2SO4
【解析】(1)因为硝酸钾中含有氮钾两种元素,所以它属于复合肥;对该题实验过程可做以下分解:①因为第一次反应生成白色沉淀和无色溶液,故可判断肯定没有CuCl2,因为有铜离子的溶液都是蓝色或蓝绿色;②加适量氯化钡溶液,生成白色沉淀A且沉淀可溶于稀硝酸,说明此白色沉淀A为BaCO3沉淀而不是BaSO4;又因为在所给的四种物质中,只有Na2CO3含有碳酸跟离子,故可判定粉末中一定有Na2CO3,一定没有Na2SO4;故无色溶液B中的溶质为NaCl,可能有KNO3;③由②的分析可知,白色沉淀A为碳酸钡,与稀硝酸反应,生成硝酸钡、水和二氧化碳气体,故可判断无色溶液C为硝酸钡溶液,无色气体D为CO2;(2)白色沉淀A的化学式为BaCO3;无色气体D的名称为二氧化碳;(3) 无色溶液B中一定含有的溶质是NaCl,可能含有的溶质是KNO3;(4)由上述实验记录推断:原粉末中一定不含Na2SO4、CuCl2。

 学习实践园地系列答案
学习实践园地系列答案【题目】小明通过实验证明二氧化碳能与氢氧化钠反应,并检验生成了碳酸盐。
25℃时,氢氧化钠和碳酸钠在乙醇中的溶解度如下表所示。
物质 | NaOH | Na2CO3 |
溶解度/g | 17.3 | <0.01 |
利用如图所示装置进行实验(该装置气密性良好;乙醇不参与反应)。
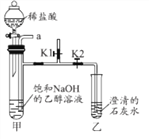
[步骤1]打开K1,关闭K2,从a口通入二氧化碳,看到饱和氢氧化钠的乙醇溶液中产生大量沉淀,停止通二氧化碳;
[步骤2]从a口通入氮气,直至排净装置中的二氧化碳;
[步骤3]关闭K1,打开K2,向甲装置的试管中滴入足量的稀盐酸。
(1)步骤1装置甲的试管中能看到沉淀的原因是______。
(2)步骤2中,排净装置甲中二氧化碳的目的是______。
(3)步骤3乙中能看到的现象是________,反应的化学方程式是_______。
【题目】甲、乙、丙、X、Y、Z六种物质间只通过一步反应就能实现右图中箭头所示的转化。不符合上述要求的一组物质是
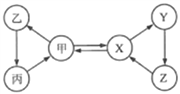
选项 | 甲 | X |
A | O2 | H2O |
B | CO2 | CaCO3 |
C | Fe | Fe3O4 |
D | NaOH | NaNO3 |
A. A B. B C. C D. D