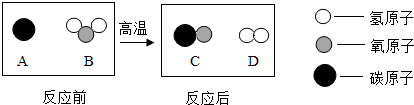
题目内容
化学方程式是重要的化学用语,正确的化学方程式是( )
A、2KClO3
| ||
| B、NaCl+H2O→NaOH+HCl | ||
C、3CO+Fe2O3
| ||
| D、2NaOH+SO2→Na2SO4+H2O |
分析:A、缺少反应条件,有些化学反应要在一定的反应条件下进行,氯酸钾制取氧气需要在二氧化锰作催化剂、加热的条件下进行;
B、化学方程式的反应物和生成物,书写位置颠倒;注意等号前为反应物,等号后为生成物;
C、3CO+Fe2O3
2Fe+3CO2;此反应的化学方程式完全正确;
D、氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,生成物的化学式书写错误,应为Na2SO3.
B、化学方程式的反应物和生成物,书写位置颠倒;注意等号前为反应物,等号后为生成物;
C、3CO+Fe2O3
| ||
D、氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,生成物的化学式书写错误,应为Na2SO3.
解答:解:A、2KClO3=2KCl+3O2↑缺少反应条件,需要在二氧化锰作催化剂、加热的条件下进行,故A错误;
B、NaCl+H2O=NaOH+HCl,反应物和生成物,书写位置颠倒;改为NaOH+HCl=NaCl+H2O,故B错误;
C、3CO+Fe2O3
2Fe+3CO2;此反应的化学方程式完全正确,故C正确;
D、生成物的化学式书写错误,应为Na2SO3.正确的化学方程式为2NaOH+SO2=Na2SO3+H2O,故D错误.
故选C.
B、NaCl+H2O=NaOH+HCl,反应物和生成物,书写位置颠倒;改为NaOH+HCl=NaCl+H2O,故B错误;
C、3CO+Fe2O3
| ||
D、生成物的化学式书写错误,应为Na2SO3.正确的化学方程式为2NaOH+SO2=Na2SO3+H2O,故D错误.
故选C.
点评:本题主要考查了根据客观事实和质量守恒定律,书写化学方程式,不能随意捏造;掌握配平化学方程式的步骤、方法、技巧.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
 海洋资源十分丰富.
海洋资源十分丰富.(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、过滤、
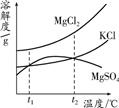
(2)晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,
如图是它们的溶解度曲线示意图.设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度大小
关系为
(3)目前世界上60%的镁是从海水中提取的.其主要步骤如下:
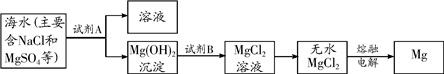
①提取Mg的过程中,试剂B选用
由无水MgCl2制取Mg的化学反应方程式为
在此过程中
②镁是重要的金属材料,广泛应用于合金、火箭和飞机制造业.镁是一种较活泼金属,在二氧化碳气体中也能燃烧.燃烧的化学方程式为:2Mg+C02═C+2MgO,反应类型属于
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为-3.据此写出该反应的化学方程式
| 实验序号 | 第一次实验 | 第二次实验 | 第三次实验 |
| 所取海水质量/kg | 100 | 100 | 100 |
| 生成沉淀质量/kg | 0.28 | 0.29 | 0.30 |
③分离出Mg(OH)2后的NaCl溶液中还含有杂质CaCl2、Na2SO4,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液和Na2CO3溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl2溶液是为了
 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如右图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题:
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,E是重要的建筑材料,F可用于清除铁锈.它们之间的转化关系如右图所示(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题: