题目内容
(2013?潮阳区模拟)结合图示实验装置,回答下列问题.

(1)用高锰酸钾固体制氧气,选用的发生装置
(2)常温下,用块状固体和液体制取气体时,用C装置(多孔隔板用来方块状固体)比B装置的优点是
(3)因为盐酸易挥发,所以实验室用盐酸制取的二氧化碳中常混有少量的氯化氢气体,为了得到干燥纯净的气体可在D中加入适当的试剂,如:除氯化氢气体通常加入饱和的碳酸氢钠溶液,那么除水蒸气应加入
(4)如果用E来收集氧气,检验气体是否已集满,应该用带火星的小木条放在
(5)化学实验的微型化有其重要的意义,既能节约药品,又能使实验中产生的污染物尽可少.a处的现象是

(1)用高锰酸钾固体制氧气,选用的发生装置
A
A
(填序号字母),装入药品前应先检查装置气密性
检查装置气密性
,反应的化学方程式是2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
(2)常温下,用块状固体和液体制取气体时,用C装置(多孔隔板用来方块状固体)比B装置的优点是
可以随时使反应停止或开始(或方便控制反应的发生与停止)
可以随时使反应停止或开始(或方便控制反应的发生与停止)
,如果实验室用二氧化锰和过氧化氢溶液来制取氧气,用C装置不能
不能
(填“能”或“不能”)起到同样的效果.(3)因为盐酸易挥发,所以实验室用盐酸制取的二氧化碳中常混有少量的氯化氢气体,为了得到干燥纯净的气体可在D中加入适当的试剂,如:除氯化氢气体通常加入饱和的碳酸氢钠溶液,那么除水蒸气应加入
浓硫酸
浓硫酸
(填试剂名称),气体应从a
a
进入(填导管口的字母).(4)如果用E来收集氧气,检验气体是否已集满,应该用带火星的小木条放在
d
d
(填导管口的字母).(5)化学实验的微型化有其重要的意义,既能节约药品,又能使实验中产生的污染物尽可少.a处的现象是
由紫色变红色
由紫色变红色
,b处的现象是澄清的石灰水变浑浊
澄清的石灰水变浑浊
,烧杯中的现象是低处的蜡烛先熄灭,高处的蜡烛后熄灭
低处的蜡烛先熄灭,高处的蜡烛后熄灭
.分析:(1)据反应物的状态和反应条件选择发生装置,装入药品前要检查装置的气密性,防止装置漏气,并据反应原理书写方程式;
(2)据装置特点分析且优越性,并据物质的状态分析可行性;
(3)浓硫酸具有吸水性,是一种常用的干燥剂,洗气装置中导管要长进短出;
(4)据氧气的密度确定进气口和排气导管,从而确定小木条的放置;
(5)据二氧化碳的性质分析解答.
(2)据装置特点分析且优越性,并据物质的状态分析可行性;
(3)浓硫酸具有吸水性,是一种常用的干燥剂,洗气装置中导管要长进短出;
(4)据氧气的密度确定进气口和排气导管,从而确定小木条的放置;
(5)据二氧化碳的性质分析解答.
解答:解:(1)加热高锰酸钾制取氧气属于固体加热型,故选发生装置A,装入药品前要检查装置的气密性,防止装置漏气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4
K2MnO4+MnO2+O2↑;
(2)用C装置(多孔隔板用来方块状固体)比B装置的优点是可通过弹簧夹的开闭随时控制反应的发生和停止,过程为:打开弹簧夹,固液接触生成气体,关闭弹簧夹,试管内气压增大,将液体压入长颈漏斗,固液分离,使反应停止;如果实验室用二氧化锰和过氧化氢溶液来制取氧气,用C装置不能起到此效果,因为二氧化锰是固体粉末,不能放于隔板上;
(3)除水蒸气应加入浓硫酸,浓硫酸是一种常用的液体干燥剂,应从a管进气,让气体与浓硫酸充分接触;
(4)氧气的密度比空气大,所以气体应从长导管进入,短导管排气,将带火星的木条放于短管d处,若木条复燃说明收集满了;
(5)二氧化碳可与水反应生成碳酸,碳酸可使紫色石蕊变红,所以a处变红,二氧化碳能与氢氧化钙反应生成不溶于水的白色沉淀碳酸钙,所以b处现象是澄清的石灰水变浑浊,二氧化碳的密度比空气大,且不能燃烧、不支持燃烧,所以c处现象是低处的蜡烛先熄灭,高处的蜡烛后熄灭;
故答案为:(1)A; 检查装置气密性;2KMnO4
K2MnO4+MnO2+O2↑;
(2)可以随时使反应停止或开始(或方便控制反应的发生与停止); 不能;
(3)浓硫酸; a;
(4)d;
(5)由紫色变红色;澄清的石灰水 变浑浊;低处的蜡烛先熄灭,高处的蜡烛后熄灭.
| ||
(2)用C装置(多孔隔板用来方块状固体)比B装置的优点是可通过弹簧夹的开闭随时控制反应的发生和停止,过程为:打开弹簧夹,固液接触生成气体,关闭弹簧夹,试管内气压增大,将液体压入长颈漏斗,固液分离,使反应停止;如果实验室用二氧化锰和过氧化氢溶液来制取氧气,用C装置不能起到此效果,因为二氧化锰是固体粉末,不能放于隔板上;
(3)除水蒸气应加入浓硫酸,浓硫酸是一种常用的液体干燥剂,应从a管进气,让气体与浓硫酸充分接触;
(4)氧气的密度比空气大,所以气体应从长导管进入,短导管排气,将带火星的木条放于短管d处,若木条复燃说明收集满了;
(5)二氧化碳可与水反应生成碳酸,碳酸可使紫色石蕊变红,所以a处变红,二氧化碳能与氢氧化钙反应生成不溶于水的白色沉淀碳酸钙,所以b处现象是澄清的石灰水变浑浊,二氧化碳的密度比空气大,且不能燃烧、不支持燃烧,所以c处现象是低处的蜡烛先熄灭,高处的蜡烛后熄灭;
故答案为:(1)A; 检查装置气密性;2KMnO4
| ||
(2)可以随时使反应停止或开始(或方便控制反应的发生与停止); 不能;
(3)浓硫酸; a;
(4)d;
(5)由紫色变红色;澄清的石灰水 变浑浊;低处的蜡烛先熄灭,高处的蜡烛后熄灭.
点评:掌握实验室制取气体的装置特点、选取方法、二氧化碳的性质、浓硫酸的性质等知识,才能依据题意正确分析解答,考查了学生对知识的掌握和应用能力.

练习册系列答案
相关题目

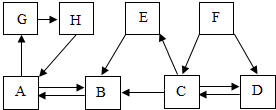 (2013?潮阳区模拟)如图所示是初中化学中几种常见物质之间的相互转化关系(部分反应物和生成物及反应条件已略去).化合物A、G、H含有相同的金属元素,在常温下,B、C为气体,B是植物光合作用的重要原料;D、F是由两种相同元素组成的无色液体,分子中的原子个数比为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液.回答下列问题:
(2013?潮阳区模拟)如图所示是初中化学中几种常见物质之间的相互转化关系(部分反应物和生成物及反应条件已略去).化合物A、G、H含有相同的金属元素,在常温下,B、C为气体,B是植物光合作用的重要原料;D、F是由两种相同元素组成的无色液体,分子中的原子个数比为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液.回答下列问题: