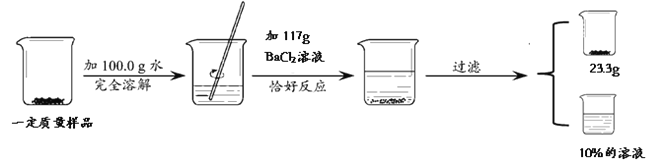
题目内容
【题目】(6分)甲、乙、丙为初中化学常见物质,他们之间有如图所示的反应
关系(“→”表示能转化,“-”表示能反应)。回答下列问题:
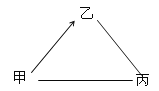
(已知CaCl2 + Na2CO3 === CaCO3 ↓+ 2NaCl)
(1)若甲、乙属于同类物质,且甲和丙反应有沉淀产生。则乙物质的
用途有 (写一种)。甲和丙反应的化学方程式为 。
(2)若甲为红色固体,则乙和足量丙反应的现象为 。
(3)若甲、乙与丙反应的产物完全相同。甲受热分解生成乙,反应的化学方程式为 。 (4)取上述甲、乙、丙中由两种或三种元素组成的物质的水溶液,将其中两种溶液混合,再加入剩余溶液中的一种,所加溶液的质量与生成沉淀的质量关系如下图所示。
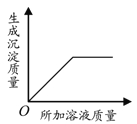
在下表中填写被混合的两种溶液及所加溶液中溶质的化学式(有几组写几组)。
混合溶液 | 所加溶液 |
【答案】(1)做干燥剂; CO2 + Ca(OH)2 ===CaCO3↓ + H2O;(2)固体消失,有气泡产生,溶液由无色变为浅绿色;(3)2NaHCO3 △ Na2CO3 + H2O + CO2↑;(4)Ca(OH)2 、NaOH——Na2CO3 ;NaOH、Na2CO3——Ca(OH)2 ;Ca(OH)2 、HCl——Na2CO3
【解析】
试题分析:(1)甲、乙属于同类物质,甲会转化成乙,且甲和丙反应有沉淀产生,乙也会与丙反应,猜想甲是氢氧化钙,乙是氢氧化钠,丙是二氧化碳,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠和氢氧化钙都是碱,都会与二氧化碳反应,且氢氧化钙和二氧化碳反应生成白色的碳酸钙沉淀,猜想正确,固体氢氧化钠具有吸水性,所以可以用作干燥剂,氢氧化钙和二氧化碳反应生成白色的碳酸钙沉淀和水;(2)甲为红色固体,甲会转化成乙,甲和乙都会与丙反应,常见的红色固体有红磷、铜、氧化铁,所以甲是氧化铁,乙是铁,氧化铁和铁都会与酸反应,丙就是盐酸或硫酸,铁与盐酸反应生成氯化亚铁和氢气,氯化亚铁在溶液中显浅绿色,反应的现象为:固体消失,有气泡产生,溶液由无色变为浅绿色;
(3)甲、乙与丙反应的产物完全相同,甲受热分解生成乙,猜想甲是碳酸氢钠,乙是碳酸钠,丙是盐酸,碳酸氢钠受热分解成碳酸钠、水和二氧化碳,碳酸钠、碳酸氢钠和盐酸反应都会生成氯化钠、水和二氧化碳,生成物相同,猜想合理,所以碳酸氢钠受热生成碳酸钠、水和二氧化碳;
(4)通过上面的推导可知,甲、乙、丙中由两种或三种元素组成的物质的水溶液,所以甲、乙、丙可以是:碳酸钠、氢氧化钠、氢氧化钙、盐酸,从沉淀出现的坐标可以看出,加入剩余溶液就出现沉淀,所以是先取出的两种溶液和后加入的只要一接触就生成沉淀,所以组合可以是:Ca(OH)2、NaOH--Na2CO3;NaOH、Na2CO3--Ca(OH)2;Ca(OH)2、HCl--Na2CO3