题目内容
 金属是一类重要的材料,人类的生活和生产都离不开金属.下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.
金属是一类重要的材料,人类的生活和生产都离不开金属.下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.(1)根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关
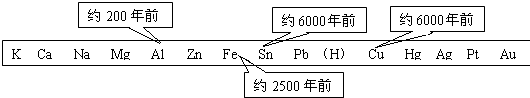
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性
(2)钢铁的生产和使用是人类文明和社会进步的一个重要标志.请你写出一氧化碳在高温条件下把铁从赤铁矿里还原出来的化学方程式
(3)每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因
分析:(1)从人类大规模开发、利用金属的年限可以看出,越活泼的金属,开发利用的越晚,说明主要和金属的活动性有关,另外,还与金属在地壳中的含量及冶炼的难易程度有关,
(2)炼铁的原理是用一氧化碳在高温条件下还原氧化铁.
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果.
(4)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑.
(2)炼铁的原理是用一氧化碳在高温条件下还原氧化铁.
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果.
(4)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑.
解答:解:
(1)金属被大规模开发、利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用,活泼金属一般以化合物形式存在,有的还比较难冶炼,其次是与该金属在地壳中的含量有关,含量越大,越容易被发现利用.
(2)一氧化碳在高温条件下把铁从赤铁矿里还原出来的化学方程式 3CO+Fe2O3
2Fe+3CO2;.
(3)铁在空气中锈蚀,实际上是铁跟 空气中的氧气、水蒸气等物质相互作用的结果,防锈的方法使其与氧气隔绝,可涂保护膜或涂油
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性.
故答案为:
(1)③
(2)3CO+Fe2O3
3CO2+2Fe,
(3)O2、H2O,在链条上涂油
(4)铝被氧化后能在表面形成一层致密的氧化物膜阻止铝进一步与空气接触
(1)金属被大规模开发、利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用,活泼金属一般以化合物形式存在,有的还比较难冶炼,其次是与该金属在地壳中的含量有关,含量越大,越容易被发现利用.
(2)一氧化碳在高温条件下把铁从赤铁矿里还原出来的化学方程式 3CO+Fe2O3
| ||
(3)铁在空气中锈蚀,实际上是铁跟 空气中的氧气、水蒸气等物质相互作用的结果,防锈的方法使其与氧气隔绝,可涂保护膜或涂油
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性.
故答案为:
(1)③
(2)3CO+Fe2O3
| ||
(3)O2、H2O,在链条上涂油
(4)铝被氧化后能在表面形成一层致密的氧化物膜阻止铝进一步与空气接触
点评:本题从金属的利用,冶炼,锈蚀及保存等方面全面考查了金属的性质,是一道不错的试题.

练习册系列答案
相关题目
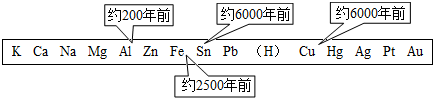


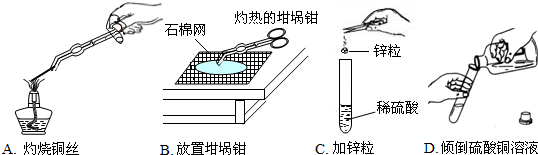
 金属是一类重要的材料,人类的生活和生产都离不开金属.
金属是一类重要的材料,人类的生活和生产都离不开金属.