题目内容
(8分)小明同学发现往水中投放过氧化钙后产生气泡。
[提出问题]产生的气体是什么呢?
[猜想假设]小明同学与本组同学讨论后认为可能是 。
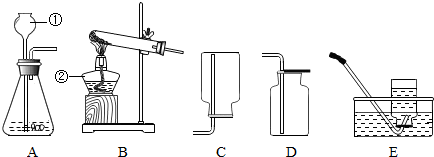
[设计实验]为研究反应后生成何种气体,小明使用如下图

甲所示的装置进行实验,打开装置中分液漏斗的活塞,控制滴加水的速度,观察到管内有气泡产生,用带火星的木条靠近气体出口处,木条复燃,说明生成的气体是 ,
假设成立。由此可知运输鱼苗时,在水中加入过氧化钙的主要目的是 。
[实验反思]根据质量守恒定律,小明认为过氧化钙与过量水反应,还会生成某种含有钙元素的生成物。开始小明假设该生成物为氧化钙,但通过思考:氧化钙能与水反应,生成氢氧化钙。他很快否定了原先的假设,并重新假设生成的含钙化合物为氢氧化钙。
(1)请写出氧化钙与水反应生成氢氧化钙的化学方程式 ,
该反应的基本类型是 。
(2)请设计一个实验方案来验证小明的新假设,并填入下表空格中:
则该实验涉及的化学反应方程式为 。
[提出问题]产生的气体是什么呢?
[猜想假设]小明同学与本组同学讨论后认为可能是 。
[设计实验]为研究反应后生成何种气体,小明使用如下图

甲所示的装置进行实验,打开装置中分液漏斗的活塞,控制滴加水的速度,观察到管内有气泡产生,用带火星的木条靠近气体出口处,木条复燃,说明生成的气体是 ,
假设成立。由此可知运输鱼苗时,在水中加入过氧化钙的主要目的是 。
[实验反思]根据质量守恒定律,小明认为过氧化钙与过量水反应,还会生成某种含有钙元素的生成物。开始小明假设该生成物为氧化钙,但通过思考:氧化钙能与水反应,生成氢氧化钙。他很快否定了原先的假设,并重新假设生成的含钙化合物为氢氧化钙。
(1)请写出氧化钙与水反应生成氢氧化钙的化学方程式 ,
该反应的基本类型是 。
(2)请设计一个实验方案来验证小明的新假设,并填入下表空格中:
| 实验步骤 | 实验现象 | 结论 |
| | | 过氧化钙与水反应,有氢氧化钙生成。 |
(共8分,每空1分)
[猜想假设]氧气(或O2)
[实验设计]氧气(或O2);
增加水中的氧气含量,供鱼苗呼吸
[实验反思]
(1)CaO+H2O ="=" Ca(OH)2 化合反应
(2)
Ca(OH)2+CO2 === CaCO3 ↓ + H2O
[猜想假设]氧气(或O2)
[实验设计]氧气(或O2);
增加水中的氧气含量,供鱼苗呼吸
[实验反思]
(1)CaO+H2O ="=" Ca(OH)2 化合反应
(2)
| 实验步骤 | 实验现象 | 结论 |
| 取反应后所得溶液(或液体)样品于试管中,然后通入CO2气体。 | 产生白色沉淀(或溶液变浑浊) | |
分析:[设计实验]根据物质的性质及带火星的木条靠导管P管口,木条复燃来判断生成的气体为氧气,根据鱼的生存需要氧气来分析向鱼塘中加入过氧化钙的目的;
[实验反思]根据氧化钙的性质来分析过氧化钙与水反应的产物,并利用氢氧化钙的性质来说明氢氧化钙的生成;
根据反应物和生成物来书写化学反应方程式,
解答:解:【实验设计】由题意可知:能使带火星的木条复燃的气体是氧气,鱼生活需要呼吸氧气,在水中加入过氧化钙的主要目的是增加水中的氧气含量,供鱼苗呼吸.
【实验反思】生石灰易与水反应生成熟石灰,CaO+H2O=Ca(OH)2.根据氢氧化钙的性质,检验氢氧化钙可用溶液中能入二氧化碳,若变浑浊,说明溶液中含有氢氧化钙;整个反应的化学方程式是2CaO2+2H2O=2Ca(OH)2+O2↑.CO2+Ca(OH)2═CaCO3↓+H20
故答案为:
【实验设计】氧气(O2)
增加水中的氧气含量,供鱼苗呼吸.
【实验反思】(1)CaO+H2O=Ca(OH)2
(2)
2CaO2+2H2O=2Ca(OH)2+O2↑.CO2+Ca(OH)2═CaCO3↓+H20
[实验反思]根据氧化钙的性质来分析过氧化钙与水反应的产物,并利用氢氧化钙的性质来说明氢氧化钙的生成;
根据反应物和生成物来书写化学反应方程式,
解答:解:【实验设计】由题意可知:能使带火星的木条复燃的气体是氧气,鱼生活需要呼吸氧气,在水中加入过氧化钙的主要目的是增加水中的氧气含量,供鱼苗呼吸.
【实验反思】生石灰易与水反应生成熟石灰,CaO+H2O=Ca(OH)2.根据氢氧化钙的性质,检验氢氧化钙可用溶液中能入二氧化碳,若变浑浊,说明溶液中含有氢氧化钙;整个反应的化学方程式是2CaO2+2H2O=2Ca(OH)2+O2↑.CO2+Ca(OH)2═CaCO3↓+H20
故答案为:
【实验设计】氧气(O2)
增加水中的氧气含量,供鱼苗呼吸.
【实验反思】(1)CaO+H2O=Ca(OH)2
(2)
| 取反应后所得溶液样品于试管中,然后通入二氧化碳气体, | 产生白色沉淀(或溶液变浑浊) |

练习册系列答案
相关题目