题目内容
为确定木炭还原氧化铜后的固体成份,请你与兴趣小组的同学完成以下探究
【对固体猜想】
猜想I:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有氧化铜、______.
【进行实验】
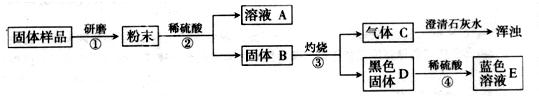
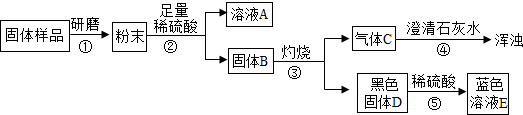
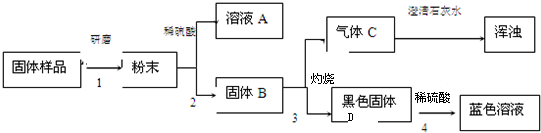
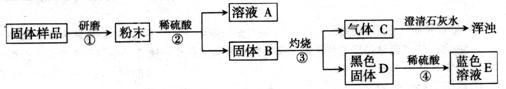
实验流程见下图:
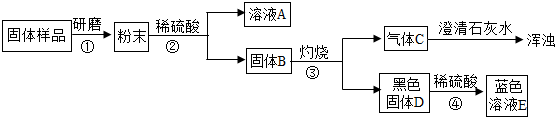
【问题与讨论】
(1)步骤②包括溶解、______两步操作.
(2)C的化学式为______,D的化学式为______,由此推出固体B中含有______(写化学式),步骤④发生反应的化学方程式为______.
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为______,说明样品中含有______,则证明猜想______成立;如果溶液A无色,则证明猜想______成立.
解:根据反应物是氧化铜和木炭,生成物的固体是铜,结合反应中的过量和不足问题,利用数学中的组合知识将三种物质任意组合,可以得到四种猜想:①全部是铜,②铜和氧化铜的混合物,③铜和木炭的混合物,④铜、氧化铜和木炭.对照题中的猜想确定答案,故答案为:木炭.
(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤操作,故答案为:过滤.
(2)根据质量守恒定律,反应物中的元素有:碳、铜、氧,结合通入石灰水后出现浑浊,可以推出C是二氧化碳,固体B灼烧后得到的黑色物质与硫酸反应会得到蓝色溶液,可以推出D是氧化铜,根据C是二氧化碳、D是氧化铜可以确定B的组成是:C、Cu.
根据反应物是硫酸和氧化铜,生成物中有硫酸铜书写化学方程式,
故答案为:CO2,CuO,C、Cu,CuO+H2SO4=CuSO4+H2O
(3)根据质量守恒定律,加入硫酸后溶液显蓝色,可知该溶液中含有硫酸铜,可知原粉末中有氧化铜,(2)推导出B中有铜,也就是原粉末中有铜,所以原粉末中有铜和氧化铜和碳,可以判断出猜想IV正确,
A是无色,说明原混合物中没有氧化铜,生成的气体C还得会使石灰水变浑浊所以猜想III正确,
故答案为:CuSO4,Cu、CuO、C,Ⅳ、Ⅲ
分析:反应物是氧化铜和碳,生成物是铜,根据数学中的组合知识,对三种物质进行组合即可得到所有的猜想,
(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤处理,
(2)我们所掌握的能使澄清石灰水变浑浊的气体是二氧化碳,与硫酸反应后,溶液显蓝色的是硫酸铜溶液.根据C、D 的现象推导出固体B的组成.
(3)加硫酸反应后溶液显蓝色,溶液中应含有硫酸铜,结合题中的现象推测样品的含量猜想的正误.
点评:在对固体猜想是要利用组合知识,总结到位,总结全面,对化学中典型的现象要加以识记,如带色的离子等.
(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤操作,故答案为:过滤.
(2)根据质量守恒定律,反应物中的元素有:碳、铜、氧,结合通入石灰水后出现浑浊,可以推出C是二氧化碳,固体B灼烧后得到的黑色物质与硫酸反应会得到蓝色溶液,可以推出D是氧化铜,根据C是二氧化碳、D是氧化铜可以确定B的组成是:C、Cu.
根据反应物是硫酸和氧化铜,生成物中有硫酸铜书写化学方程式,
故答案为:CO2,CuO,C、Cu,CuO+H2SO4=CuSO4+H2O
(3)根据质量守恒定律,加入硫酸后溶液显蓝色,可知该溶液中含有硫酸铜,可知原粉末中有氧化铜,(2)推导出B中有铜,也就是原粉末中有铜,所以原粉末中有铜和氧化铜和碳,可以判断出猜想IV正确,
A是无色,说明原混合物中没有氧化铜,生成的气体C还得会使石灰水变浑浊所以猜想III正确,
故答案为:CuSO4,Cu、CuO、C,Ⅳ、Ⅲ
分析:反应物是氧化铜和碳,生成物是铜,根据数学中的组合知识,对三种物质进行组合即可得到所有的猜想,
(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤处理,
(2)我们所掌握的能使澄清石灰水变浑浊的气体是二氧化碳,与硫酸反应后,溶液显蓝色的是硫酸铜溶液.根据C、D 的现象推导出固体B的组成.
(3)加硫酸反应后溶液显蓝色,溶液中应含有硫酸铜,结合题中的现象推测样品的含量猜想的正误.
点评:在对固体猜想是要利用组合知识,总结到位,总结全面,对化学中典型的现象要加以识记,如带色的离子等.

练习册系列答案
相关题目