题目内容
【题目】为了测定某钢铁样品(主要成分是铁,少量的碳,其他杂质忽略不计)中碳的质量分数,现取一定质量的废钢粉末,向其中逐滴加入稀硫酸,至刚好不再产生气泡,用去稀硫酸100g,过滤、洗涤、干燥,得滤渣0.1g,生成氢气0.3g,求:
(1)所取样品中铁的质量。
(2)该样品中碳的质量分数(精确到0.1%)。
(3)稀硫酸的质量分数。
【答案】(1)8.4g(2)1.2%(3)14.7%
【解析】
铁和稀硫酸反应生成硫酸亚铁和氢气。
(1)设反应的铁的质量是x,稀硫酸的质量是y
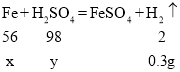
![]()
x=8.4g
![]()
y=14.7g
(2)钢铁中不反应的是碳,故残渣0.1g即为碳的质量,故该样品中碳的质量分数为![]() ×100%≈1.2%
×100%≈1.2%
(3)稀硫酸的质量分数为:![]() ×100%=14.7%
×100%=14.7%
答:所取样品中铁的质量是8.4g,该样品中碳的质量分数是1.2%,稀硫酸的质量分数是14.7%。

【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
加入稀盐酸的质量/g | 生成气体的总质量/g | |
第1次 | 20 | 1.1 |
第2次 | 20 | 2.2 |
第3次 | 20 | m |
第4次 | 20 | 4.4 |
第5次 | 20 | 4.4 |
(1)m的值为_________g
(2)12g石灰石样品中碳酸钙的质量等于_________g
(3)反应完全后最终溶液中氯化钙的质量分数为_______?(写出计算过程,计算结果精确至0.1)
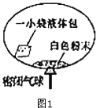
【题目】某研究小组对自动充气气球(如图1)进行下探究。
(查阅资料)
①该气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧 化碳气体,实现气球自动充气。
②氯化钙水溶液呈中性,碳酸钠、碳酸氢钠的水溶液均呈碱性。
③用一定溶质质量分数的 NaHCO3和Na2CO3溶液进行实验,实验现象记录如下:
NaHCO3溶液 | Na2CO3溶液 | |
加入澄清石灰水 | 溶液变浑浊 | 溶液变浑浊 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
探究1:气体的成分
为检验气体是二氧化碳,可选用______(填试剂名称).
探究2:液体包内溶液的酸碱性
室温时,用 pH试纸测得溶液的 pH 的方法是____;若 测得溶液的 pH=3,则该溶液呈___性。
探究 3:白色粉末的成分
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学 认为是碳酸钠和碳酸氢钠的混合物。
(进行实验)
(1)将少量白色粉末放入水中搅拌,观察到______,说明甲同学的猜想不正确。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的
10%的盐酸(装置如图2),记录如下表:


(解释与结论)
(1)实验Ⅰ的化学方程式为__________。
(2)表中a=_______;V1________V2(填“>”、“<”或“=”)。
(3)上述实验得出的结论及判断依据是__________。
(反思与评价)老师指出还可以采用更简单的方法得出与上述实验(2)相同的结论,实验方案为____。