题目内容
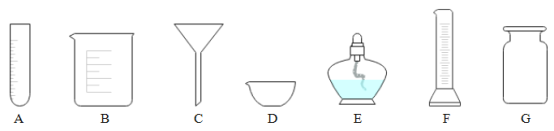
【题目】图1所示为实验室中常见的气体制备和收集装置。
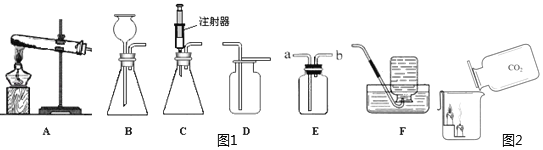
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置_____(填字母序号),反应的化学方程式为_____。若用装置D收集氧气,验满的方法是_____。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是_____。
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从_____(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从_____(填“a”或“b”)端通入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中_____装置(填字母序号)。
(5)将二氧化碳气体通入紫色石蕊试液中,石蕊试液变红色,反应原理用化学方程式表示为_____。
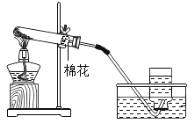
(6)如图2所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的化学性质是_____。
【答案】A 2KMnO4![]() K2MnO4+MnO2+O2↑ 将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了 可以控制反应的速率 a b F CO2+H2O=H2CO3 二氧化碳既不能燃烧,也不能支持燃烧
K2MnO4+MnO2+O2↑ 将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了 可以控制反应的速率 a b F CO2+H2O=H2CO3 二氧化碳既不能燃烧,也不能支持燃烧
【解析】
(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
K2MnO4+MnO2+O2↑;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,C的优点是:可以控制反应的速率;
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从长管进入,因为二氧化碳的密度比空气大;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b(短)管进入,因为氧气的密度比水小;
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,因此只能用排水法收集,故选F;
(5)将二氧化碳气体通入紫色石蕊试液中,石蕊试液变红色,因为二氧化碳和水反应生成碳酸;反应的化学方程式为:CO2+H2O=H2CO3;
(6)如图2所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的化学性质是:二氧化碳既不能燃烧,也不能支持燃烧。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】一种含碳酸钙的“石头纸”越来越流行,为测定碳酸钙的含量,课外活动小组同学称取50g碎纸样品,分别在5只烧杯中进行实验,实验数据见表(假设纸张其他成分既不溶于水,也不与稀盐酸反应)。
烧杯① | 烧杯② | 烧杯③ | 烧示④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 3.52 |
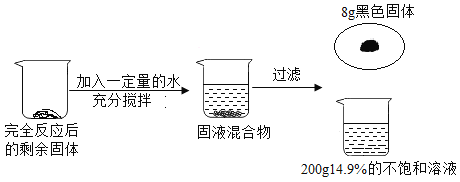
(1) 10g样品与足量稀盐酸反应最多生成_____g气体;
(2)求样品中碳酸钙的质量分数_____。
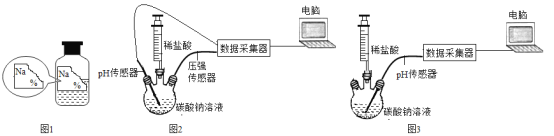
【题目】实验室有一瓶常用的无色溶液标签模糊了(如图1)。为确定该瓶溶液的溶质是什么,同学们进行了如下探究。
(提出问题)这瓶溶液中的溶质是什么?
(提出猜想)猜想1:可能是氢氧化钠;
猜想2:可能是碳酸氢钠;
猜想3:可能是碳酸钠;
猜想4:可能是氯化钠。
查阅资料)①碳酸氢钠稀溶液显碱性;②碳酸氢钠稀溶液不与氯化钙稀溶液反应。
(实验探究)
实验设计 | 实验现象 | 实验结论 |
小亮同学取2mL该无色溶液于试管中,滴入2滴无色酚酞试液 | 溶液变红 | 猜想1正确,猜想4不正确 |
小丽同学取2mL该无色溶液与试管中,倒入3mL稀盐酸 | 立即产生气泡 | 猜想_____不正确 |
(交流讨论)
(1)同学们一致认为小亮同学的实验结论不严谨,请说出理由:_____。
(2)为确定无色溶液到底是什么,小强同学继续进行了如下实验:
①取2mL该无色溶液于试管中,滴入稀氯化钙溶液,边加边震荡,观察到_____现象。由此得出猜想3正确,请写出该反应的化学方程式:_____。
②另取2mL该无色溶液于试管中,逐滴加入稀盐酸,一段时间后,才观察到有气泡产生。
小丽和小强都是向无色溶液中加入稀盐酸,为什么现象不尽相同呢?
(延伸探究)在老师的指导下,小强和小丽分别用下面的数字化技术分别测量密闭容器中碳酸钠溶液、碳酸氢钠溶液与稀盐酸反应的装置(所用的碳酸钠溶液、碳酸氢钠溶液浓度相同,稀盐酸的浓度也相同)。
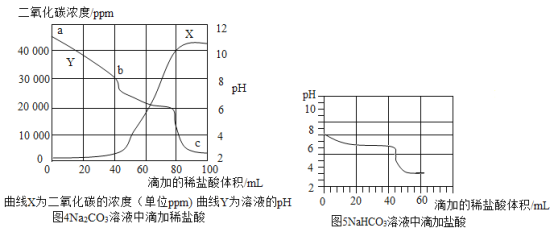
小强和小丽分别从注射器中缓慢滴入盐酸,记录数据。小强用图2装置得到的数据如图4,小丽用图3装置得的数据如图5。
(交流评价)
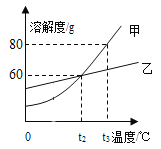
(3)由图4图5可知,所用两种溶液碱性强的是_____(写化学式)。
(4)c点的溶质是_____。
(5)将图5和图4阴影部分进行叠加,发现两者基本重合,判断b点的溶质是_____和_____。此结论可以解释小强第二次实验开始时无明显气泡产生的原因。
(6)由图4可知,当稀盐酸加至80mL时,Na2CO3恰好完全反应。此时溶液的pH小于7,原因是_____。