题目内容
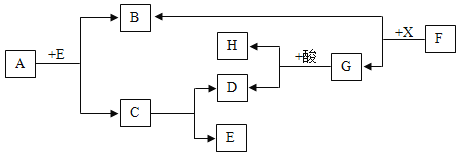
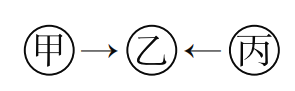
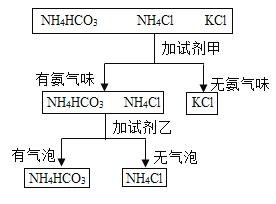
【题目】某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥,过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:稀盐酸,乙:熟石灰
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:稀硫酸
【答案】D
【解析】
在NH4HCO3、NH4Cl、KCl三种化肥中,NH4HCO3和NH4Cl都含有铵根,属于铵态氮肥,KCl中没有铵根,铵态氮肥遇碱会产生具有刺激性气味的氨气。在这三种化肥中分别加入试剂甲后,在NH4HCO3和NH4Cl有氨味产生,KCl中没有,则加入的试剂甲应该是碱;在NH4HCO3和NH4Cl中分别加入试剂乙后,在NH4HCO3有气泡产生,而NH4Cl没有气泡产生,NH4HCO3中含有碳酸氢根,遇酸会产生二氧化碳气体,则乙应该是酸。故选D。

 名校课堂系列答案
名校课堂系列答案【题目】小组同学在探究金属与酸反应时,将铝片、锌片打磨后,分别投入盛有等体积、等浓度稀盐酸的试管中,观察到铝与稀盐酸反应较锌与稀盐酸反应快。
【提出问题】金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
【猜想与假设】a.可能与盐酸的浓度有关;b. 可能与反应时的温度有关。
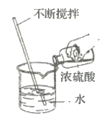
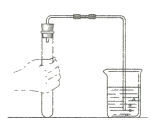
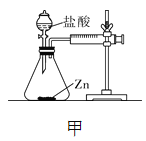
【设计并实验】小明利用如图甲所示装置,用不同质量分数的盐酸和相同形状的锌片进行如下实验。
实验编号 | 盐酸的质量分数(均取20 mL) | 温度/℃ | 记录的数据 |
① | 5% | 30 | |
② | 10% | 20 | |
③ | 5% | 20 | |
④ | 10% | 30 |
【讨论】(1)写出锌与稀盐酸反应的化学方程式__________。
(2)实验时,需将金属片打磨,其目的是__________。
(3)实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是______________。
【分析数据、得出结论】
(4)实验中记录的数据可能是_____________。
(5)对比实验________可知温度对金属与酸反应的速率的影响。
(6)实验表明,四次实验时,反应的速率由快到慢依次为④、②、①、③。根据记录的数据分析,如果盐酸质量分数为10%,温度为25℃,则所记录数据应该介于哪两次实验所记录的数据之间?________________________。
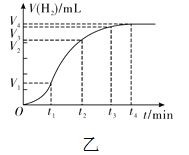
【拓展】进行锌与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳锌与稀盐酸反应速率的变化规律______________,结合上述探究解释曲线变化的原因 ________________________________。