题目内容
【题目】用数字或化学用语符号填空:
(1)2个氮分子_____;
(2)3个硝酸根离子_____;
(3)地壳中含量最多的金属元素_____;
(4)算出氧化铁中氧元素的质量分数:_____;
(5)画出硅原子的结构示意图:_____;
(6)硫酸铵的化学式_____。
【答案】2N2 3NO3﹣ Al 30%  (NH4)2SO4
(NH4)2SO4
【解析】
(1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字。
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。
(3)地壳中含量最多的金属元素是铝元素,进行分析解答。
(4)根据化合物中元素的质量分数=![]() ×100%,进行分析解答。
×100%,进行分析解答。
(5)硅原子核内有14个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子,画出即可。
(6)硫酸铵中铵根显+1价,硫酸根显﹣2价,写出其化学式即可。
(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则2个氮分子可表示为:2N2。故填:2N2
(2)由离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字,故3个硝酸根离子可表示为:3NO3﹣。故填:3NO3﹣
(3)地壳中含量最多的金属元素是铝元素,其元素符号为:Al。故填:Al
(4)氧化铁中氧元素的质量分数为![]() ×100%=30%。故填:30%
×100%=30%。故填:30%
(5)硅原子核内有14个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子,其原子结构示意图为: 。故填:
。故填:
(6)硫酸铵中铵根显+1价,硫酸根显﹣2价,其化学式为:(NH4)2SO4。故填:(NH4)2SO4

【题目】质量守恒定律的发现对化学的发展作出了重要贡献。
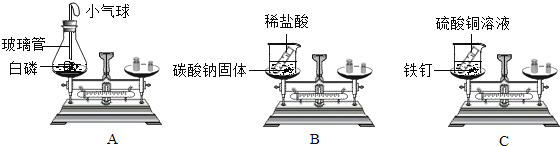
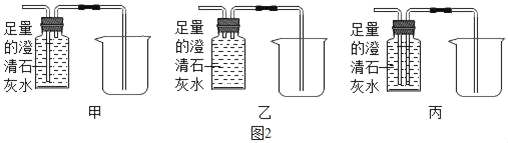
(1)用如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是_____(填序号),理由是_____。
(2)从微观角度分析有助于我们理解质量守恒定律,在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生化学反应,经过一段时间后停止反应,其中A、B、C、D的微观示意图和反应前后各物质的质量如表所示。
物质 | A | B | C | D |
|
微观示意图 |
|
|
|
| |
反应前质量/g | 100 | 20 | x | y | |
反应后质量/g | 32 | 140 | 126 | 46 |
①从微观角度分析,化学反应中质量守恒的原因是_____。
②该反应中B和C的质量比为_____。
③表中x的值是_____。