题目内容
(2011?丰台区二模)小丽来到实验室,看到实验桌上有一瓶敞口放置的氢氧化钠固体,于是对其是否变质产生了兴趣.她和同学们准备对这瓶固体进行探究.查阅资料:a.碳酸钠溶液显碱性,氯化钙溶液呈中性.
b.碳酸钠溶液与氯化钙溶液可以发生反应:Na2CO3+CaCl2=CaCO3↓+2NaCl.
作出猜想:
猜想1.固体没有变质
猜想2.固体部分变质
猜想3.______
设计方案:
| 实验操作 | 实验现象 | 实验结论 | |
| 方案一 | 取少量固体放入试管中,滴加几滴稀盐酸 | 无明显现象 | 猜想1正确 |
| 方案二 | 取少量固体放入试管中加水溶解,滴加足量澄清石灰水 | 产生白色沉淀 | 猜想2正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | 溶液变为红色 |
方案二不合理的原因是______.同学们重新设计了方案并进行了实验.
实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放入试管中加水溶解,滴加足量______ | 产生白色沉淀 | 猜想2正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | ______ |
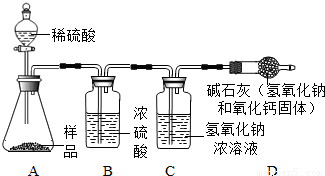
继续探究:同学们继续探究该氢氧化钠固体样品中碳酸钠的质量分数.利用以下装置进行了实验.
你认为她们需要测的数据是______(填字母序号).
a.固体样品的质量 b.碱石灰实验前后的质量
c.浓硫酸实验前后的质量 d.氢氧化钠溶液实验前后的质量
e.所用稀硫酸的质量
实验反思:根据所得数据进行计算发现结果比实际偏小,原因可能是______.
【答案】分析:【作出猜想】根据氢氧化钠易和空气中的二氧化碳反应生成碳酸钠来解答;
【设计方案】根据碳酸钠与氢氧化钠的性质解答;
【实验探究】根据碳酸钠与氯化钙反应及氢氧化钠溶液呈碱性来解答;
【继续探究】氢氧化钠固体样品中碳酸钠的质量分数: 100%来解答.
100%来解答.
解答:解:【作出猜想】氢氧化钠易和空气中的二氧化碳反应生成碳酸钠,该固体有三种可能:①没有变质,是氢氧化钠,②部分变质,是氢氧化钠和碳酸钠的混合物,③完全变质,是碳酸钠;所以猜想3为固体完全变质;
【设计方案】方案一、取少量固体放入试管中,滴加几滴稀盐酸,无明显现象,不能证明固体没有变质,因为若样品变质,加入的少量稀盐酸先与NaOH反应,无明显现象;若样品完全变质,加入的几滴稀盐酸与Na2CO3反应,产生NaHCO3,也无明显现象,所以方案一不合理;
方案二、取少量固体放入试管中加水溶解,滴加足量澄清石灰水,有白色沉淀生成,证明样品中一定有碳酸钠,样品变质,碳酸钠溶液为碱性,滴加酚酞试液变红色,所以取上层清液放入另一只试管中,滴加酚酞溶液,溶液变红色,不能证明溶液中有氢氧化钠,所以方案二不合理;
【实验探究】
取少量固体放入试管中加水溶解,滴加足量CaCl2溶液,产生白色沉淀,证明样品中一定有碳酸钠,取上层清液放入另一只试管中,滴加酚酞溶液,溶液由无色变成红色,证明样品中有氢氧化钠,固体部分变质,猜想2正确;
若猜想3正确该实验现象是:取少量固体放入试管中,滴加足量CaCl2后产生白色沉淀;取上层清液放入另一只试管中,滴加酚酞溶液后不变色;
【继续探究】氢氧化钠固体样品中碳酸钠的质量分数: 100%,
100%,
要计算碳酸钠的质量分数,需要知道固体样品质量和样品中碳酸钠的质量,碳酸钠质量不易测出,可根据氢氧化钠溶液实验前后的质量,求出生成的二氧化碳质量,进而求出碳酸钠质量;
【实验反思】根据所得数据进行计算发现结果比实际偏小,原因可能是:A、B容器内还有剩余的CO2没有完全被氢氧化钠吸收,致使求出的碳酸钠质量分数偏小.
故答案为:
【作出猜想】固体完全变质;
【设计方案】
方案一:若样品变质,加入的少量稀盐酸先与NaOH反应,无明显现象;若样品完全变质,加入的几滴稀盐酸与Na2CO3反应,产生NaHCO3,也无明显现象;
方案二:碳酸钠与石灰水反应产生的氢氧化钠也能使滤液中的酚酞变红;
【实验探究】
取少量固体放入试管中,滴加足量CaCl2后产生白色沉淀;取上层清液放入另一只试管中,滴加酚酞溶液后不变色;
【继续探究】ad;
A、B容器内还有剩余的CO2没有完全被氢氧化钠吸收.
点评:本题考查了学生“NaOH溶液吸收空气中的CO2生成Na2CO3;Na2CO3溶液中加入钙盐溶液生成CaCO3白色沉淀和酚酞试液变色”的一些知识,题目通过药品是否变质的探究培养了学生的实验探究能力.
【设计方案】根据碳酸钠与氢氧化钠的性质解答;
【实验探究】根据碳酸钠与氯化钙反应及氢氧化钠溶液呈碱性来解答;
【继续探究】氢氧化钠固体样品中碳酸钠的质量分数:
 100%来解答.
100%来解答.解答:解:【作出猜想】氢氧化钠易和空气中的二氧化碳反应生成碳酸钠,该固体有三种可能:①没有变质,是氢氧化钠,②部分变质,是氢氧化钠和碳酸钠的混合物,③完全变质,是碳酸钠;所以猜想3为固体完全变质;
【设计方案】方案一、取少量固体放入试管中,滴加几滴稀盐酸,无明显现象,不能证明固体没有变质,因为若样品变质,加入的少量稀盐酸先与NaOH反应,无明显现象;若样品完全变质,加入的几滴稀盐酸与Na2CO3反应,产生NaHCO3,也无明显现象,所以方案一不合理;
方案二、取少量固体放入试管中加水溶解,滴加足量澄清石灰水,有白色沉淀生成,证明样品中一定有碳酸钠,样品变质,碳酸钠溶液为碱性,滴加酚酞试液变红色,所以取上层清液放入另一只试管中,滴加酚酞溶液,溶液变红色,不能证明溶液中有氢氧化钠,所以方案二不合理;
【实验探究】
取少量固体放入试管中加水溶解,滴加足量CaCl2溶液,产生白色沉淀,证明样品中一定有碳酸钠,取上层清液放入另一只试管中,滴加酚酞溶液,溶液由无色变成红色,证明样品中有氢氧化钠,固体部分变质,猜想2正确;
若猜想3正确该实验现象是:取少量固体放入试管中,滴加足量CaCl2后产生白色沉淀;取上层清液放入另一只试管中,滴加酚酞溶液后不变色;
【继续探究】氢氧化钠固体样品中碳酸钠的质量分数:
 100%,
100%,要计算碳酸钠的质量分数,需要知道固体样品质量和样品中碳酸钠的质量,碳酸钠质量不易测出,可根据氢氧化钠溶液实验前后的质量,求出生成的二氧化碳质量,进而求出碳酸钠质量;
【实验反思】根据所得数据进行计算发现结果比实际偏小,原因可能是:A、B容器内还有剩余的CO2没有完全被氢氧化钠吸收,致使求出的碳酸钠质量分数偏小.
故答案为:
【作出猜想】固体完全变质;
【设计方案】
方案一:若样品变质,加入的少量稀盐酸先与NaOH反应,无明显现象;若样品完全变质,加入的几滴稀盐酸与Na2CO3反应,产生NaHCO3,也无明显现象;
方案二:碳酸钠与石灰水反应产生的氢氧化钠也能使滤液中的酚酞变红;
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| CaCl2溶液 | ||
| 溶液由无色变为变红色 |
【继续探究】ad;
A、B容器内还有剩余的CO2没有完全被氢氧化钠吸收.
点评:本题考查了学生“NaOH溶液吸收空气中的CO2生成Na2CO3;Na2CO3溶液中加入钙盐溶液生成CaCO3白色沉淀和酚酞试液变色”的一些知识,题目通过药品是否变质的探究培养了学生的实验探究能力.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目
(2011?丰台区二模)牙膏是我们不可缺少的日用品.
(1)生活中使用的加氟牙膏中的“氟”是指(填“原子”或“元素”).
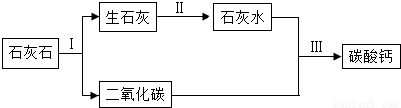
(2)牙膏中的摩擦剂是极细小的碳酸钙粉末,它的生产过程如右图所示:
①步骤Ⅰ的基本反应类型为.
②步骤Ⅱ发生反应的化学方程式为.
(3)右图牙膏说明书中,单氟磷酸钠(Na2PO3F)由种元素组成.该牙膏中单氟磷酸钠(相对分子质量为144)的质量分数为(结果保留两位小数).
(1)生活中使用的加氟牙膏中的“氟”是指(填“原子”或“元素”).
(2)牙膏中的摩擦剂是极细小的碳酸钙粉末,它的生产过程如右图所示:
①步骤Ⅰ的基本反应类型为.
②步骤Ⅱ发生反应的化学方程式为.
(3)右图牙膏说明书中,单氟磷酸钠(Na2PO3F)由种元素组成.该牙膏中单氟磷酸钠(相对分子质量为144)的质量分数为(结果保留两位小数).
| 牙膏说明书 主要活性成分:单氟磷酸钠 (Na2PO3F) 牙膏质量:100g 含 氟:100mg 功 效:预防蛀牙 |

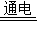 2NaOH+Cl2↑+H2↑.若制得40g氢氧化钠,同时可得到氢气的质量是多少?
2NaOH+Cl2↑+H2↑.若制得40g氢氧化钠,同时可得到氢气的质量是多少?