题目内容
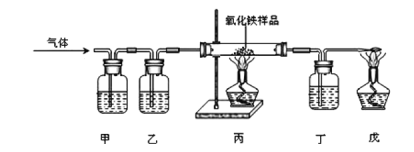
【题目】夏飞同学想要用含有杂质二氧化碳、氢气和水蒸气的一氧化碳气体测定mg样品中氧化铁的质量分数。装置如图所示,连接实验装置后先通一段时间氮气,再继续实验(已知试剂均足量,样品中的杂质不参与反应也不挥发)。下列说法正确的是( )
①装置甲、乙、丁中的试剂分别是浓硫酸、氢氧化钠溶液、澄清石灰水; ②实验时先点燃丙、戊处的酒精灯,过一会再通入混合气体; ③该实验既可验证一氧化碳的还原性,又可验证一氧化碳的可燃性; ④实验中会观察到甲、丁中液体均变浑浊; ⑤实验结束后称量丙中固体质量为ng,则样品中氧化铁的质量分数为10(m-n)/3m×100﹪ ⑥利用丁装置在反应前后改变的质量也能计算出氧化铁的质量分数
A. ①②③⑤B. ②③⑤C. ②③④⑤D. ③④⑤⑥
【答案】B
【解析】
①乙装置中不能是氢氧化钠溶液,因为气体经过氢氧化钠溶液后会有水分带出,故错误;②该实验中有一氧化碳参与反应,为了防止一氧化碳污染空气,故要先点燃两处酒精灯,故正确;③该实验中丁处的澄清石灰水变浑浊,丙中的氧化铁变为红色,体现了一氧化碳的还原性,尾气处一氧化碳燃烧,体现了一氧化碳的可燃性,故正确;④甲中是为了除去二氧化碳,故应该用氢氧化钠,故不变浑浊,故错误;⑤设样品中氧化铁的质量为x,根据原子守恒,氧化铁与铁存在下列关系:

![]() 得x=
得x=![]() (m-n)
(m-n)
故样品中氧化铁的质量分数为: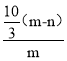 ×100%=
×100%=![]() ×100%,故正确;
×100%,故正确;
⑥丁装置中的水分部分被带出,故不能计算,故错误。故选B。

 名校课堂系列答案
名校课堂系列答案【题目】学校化学兴趣小组同学为测定野外采集到的石灰石中碳酸钙的质量分数。称取10.0g 的石灰石样品,把 100g 稀盐酸分 5 次加入样品中(假设杂质不反应也不溶解),得实验数据如下
滴加次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
稀盐酸的用量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体质量/g | 7.5 | x | 2.5 | 2.0 | 2.0 |
请计算:
(1)表中 x 的数值是________;
(2)这种石灰石样品中碳酸钙的质量分数是________;
(3)这些样品完全反应共产生气体的质量是多少_________?(写出规范的计算过程)
【题目】发酵粉的主要成分中含有碳酸氢钠。某化学兴趣小组的同学对碳酸氢钠的性质进行如下探究。
Ⅰ.定性探究
实验一:探究碳酸氢钠溶液的酸碱性
(1)用pH试纸测得碳酸氢钠溶液的pH约为9,可知碳酸氢钠溶液________性。
实验二:探究碳酸氢钠的热稳定性
[查阅资料] 碳酸氢钠受热容易分解,生成水、一种气体和一种常见的固体物质。
[实验1] 如图所示,取一定量的碳酸氢钠放到铜片上加热。

(2)加热一段时间后,观察到烧杯内壁产生___________(填现象)。
(3)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊,说明该气体是______________。
(4)欲通过实验探究进一步确定充分加热后的固体产物的成分。
猜想1:可能是NaOH;猜想2:可能是Na2CO3;猜想3:可能是NaOH和Na2CO3。
实验2:
实验操作(步骤) | 实验现象 | 实验结论 |
①将该固体溶于水配制成溶液,取少量溶液于试管中,滴加足量稀盐酸 | 有气体产生 | 猜想_______不成立 |
②另取少量溶液于试管中,滴加_____ | _____ | 固体产物中含Na2CO3 |
③取步骤②所得上层清液,滴加_____ | 无明显现象 | 猜想2成立 |
[实验结论]
(5)NaHCO3受热易分解,反应化学方程式为_________________________________________。
Ⅱ.定量探究
为测定某发酵粉中碳酸氢钠的质量分数(发酵粉中其他组分不参与反应),设计了如下实验。
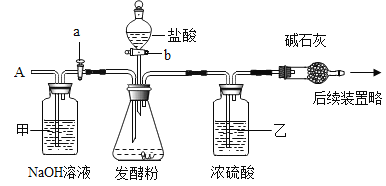
[查阅资料] 碱石灰是氧化钙和氢氧化钠固体的混合物。
[实验步骤]
①取50g样品于锥形瓶中,关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量空气;
②关闭活塞a,打开活塞b,加入足量的稀盐酸,直至锥形瓶内不再产生气泡;
③关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量空气,直至干燥管内物质质量不再增加;
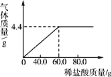
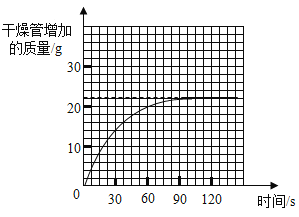
④测量干燥管增加的质量与时间关系(见曲线图)。
(1)步骤①加入样品前还应___________________。
(2)装置乙的作用是_________________________。
(3)步骤③鼓入一定量空气的目的是_________________________________。
(4)若缺少装置甲,将导致结果_________(选填“偏大”、“偏小”或“不变”)。
(5)实验测得干燥管增加的质量与时间关系(见曲线图),涉及反应的方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑。请回答:
①生成二氧化碳的质量为_______g。
②该样品中碳酸氢钠的质量分数。(写出计算过程)______。
(6)[拓展应用]
①碳酸氢钠、氢氧化镁、氢氧化铝等常用于制作抗酸药,用来治疗胃酸过多。但对于患有胃溃疡(胃黏膜溃烂)的病人在胃酸过多时,却不宜服用碳酸氢钠,其原因是____________________。
②实验室有两瓶失去标签的固体药品,已知它们是碳酸钠和碳酸氢钠,你能否设计一个实验进行鉴别,请简述你的实验方案、现象和结论______________________________________________。