题目内容
【题目】某学习小组测定某工业废水(含有H2SO4、HNO3,不含固体杂质)中H2SO4的含量。取100g废水于烧杯中,加入100gBaCl2溶液,恰好完全反应,经过滤得到176.7g溶液。(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为________________g。
(2)该工业废水中硫酸的质量分数为_______________。(写出计算过程,计算结果精确到0.1%;方程式:![]() )
)
【答案】23.3g 9.8%(详见解析)
【解析】
(1)硫酸与氯化钡反应生成硫酸钡的沉淀和硝酸。由质量守恒定律可知,生成沉淀的质量=100g+100g-176.7=23.3g;
(2)设废水中硫酸的质量分数为x
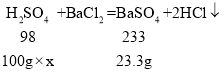
![]()
x=9.8%
答:(1)充分反应后生成沉淀的质量为23.3g;
(2)该工业废水中硫酸的质量分数为9.8%。

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目