题目内容
【题目】从微观的角度了解物质极其变化,有助于更好的认识物质组成和变化的本质。
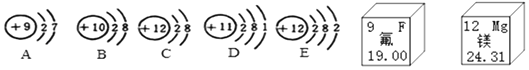
(1)已知A的相对原子质量为19,粒子A核内中子数为_____,A与E形成化合物的化学式为_____。
(2)粒子A、B、C、D、E中,属于同一种元素的是_____(填序号),属于第二周期的元素共_____种。
(3)D、E化学性质不同的原因是_____。
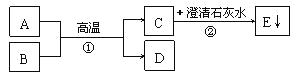
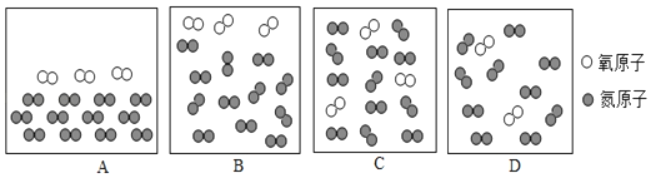
(4)如图为两种化合物在一定条件下发生反应的微观示意图:
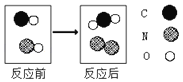
①该反应的化学方程式为_____。
②上述反应中,作为还原剂的物质是_____(填物质化学式);化合价升高的元素是_____(填元素符号)。
【答案】10 ,MgF2 CE; 2 最外层电子数不同 2 CO+2NO=2CO2 +N2 CO C
【解析】
(1)已知A的相对原子质量为19,且其质子数为9,根据相对原子质量≈质子数+中子数,所以粒子A核内中子数为19﹣9=10,A为氟,常见化合价为﹣1价,而E为镁元素,最外层两个电子,所以化合价一般为+2价,A与E形成化合物的化学式为 MgF2 。
(2)元素是具有相同质子数即核电荷数的同一类原子的总称,粒子A、B、C、D、E中,所以属于同一种元素的是 C与E,原子的电子层数决定周期数,属于第二周期的是原子的电子层数为两层的,所以属于第二周期的元素是A、B,共 2种。
(3)原子的最外层电子数相同,元素的化学性质相似,D、E化学性质不同的原因是最外层电子数不同。
(4)①根据发生反应的微观示意图可知,该反应的化学方程式为 2CO+2NO=2CO2 +N2。
②化学反应中,得到氧元素的反应物是还原剂,该反应中还原剂是 CO;反应中碳元素由反应前的+2价变成反应后的+4价,所以化合价升高的元素是 C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目