题目内容
【题目】依据所学化学知识回答:
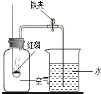
(1)据报道:上海世博停车场安装催化光解设施,可将汽车尾气中的CO和NO2转化成CO2和空气中含量最多的气体。写出该反应的化学方程式 。
(2)空气中CO2含量增多是造成温室效应的主要原因。科学家正在研究将CO2加氢转化成甲烷(CH4)、甲酸(CH2O2)等化工原料,甲烷、甲酸属于 化合物(填“无机”或 “有机”)。
(3)卫生部推广使用强化加铁酱油。这里的“铁”指的是 (填“单质”“元素”或“原子”)。
(4)小明晚上切完西瓜后就将刀放在菜板上,第二天早上发现刀生锈了。刀生锈的原因是铁与空气中的 和 等共同作用的结果。
(5)蚊子等昆虫叮咬人时,会向人体射入一种叫蚁酸的酸性物质,使皮肤红肿、痛痒,可涂肥皂水止痒,是因为肥皂水的PH 7(填“>”或“<”或“=”)。
(6)洪灾过后,卫生防疫工作人员对死亡的动物尸体撒泼一定的熟石灰并深埋。熟石灰的主要作用是 (填序号)。
A.中和作用 B.杀菌消毒 C.标记作用
【答案】(1)![]() (2)有机 (3)元素 (4)O2、H2O (5) > (6)B
(2)有机 (3)元素 (4)O2、H2O (5) > (6)B
【解析】
(1)根据“停车场安装催化光解设施”一句确定反应条件,根据“CO和NO2转化成CO2和空气中含量最多的气体”确定反应物和生成物,再写出该反应的化学方程式;
(2)根据有机物的概念考虑;
(3)在强化加铁酱油中,铁是以无机盐的形式存在的,这里的铁指铁元素.
(4)根据铁生锈的条件分析判断;
(5)肥皂水显碱性;
(6)可以抑制多数细菌的繁殖,避免瘟疫发生.
解答:解:(1)根据“停车场安装催化光解设施”一句话可知反应条件是阳光和催化剂,根据“CO和NO2转化成CO2和空气中含量最多的气体”可知生成物是二氧化碳和氮气,再根据化学方程式的配平,正确写出该反应的化学方程式为:
4CO+2NO2![]() 4CO2+N2;
4CO2+N2;
(2)含碳的化合物是有机化合物,甲烷(CH4)、甲酸(CH2O2)符合有机物的概念,是有机化合物;
(3)在强化加铁酱油中,铁是以无机盐的形式存在的,这里的铁指铁元素;
(4)铁在潮湿的空气中,与水和氧气反应生成铁锈,其主要成分是氧化铁;
(5)肥皂水显碱性,其pH值>7;
(6)熟石灰显碱性,可以抑制多数细菌的繁殖,避免瘟疫发生,主要作用是杀菌消毒;
故答案为:
(1)4CO+2NO2![]() 4CO2+N2;
4CO2+N2;
(2)有机;
(3)元素;
(4)O2;H2O;
(5)>;
(6)B.

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
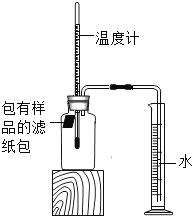
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
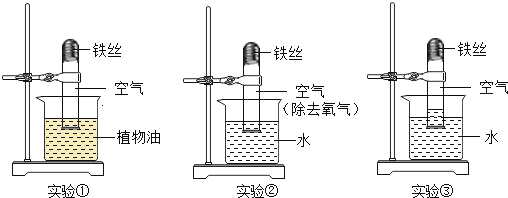
【题目】请你参与以下2个实验探究活动并回答其中的问题。
Ⅰ SO2和Cl2均能将湿润的有色物质漂白成无色物质。某兴起小组为验证SO2和Cl2的漂白性,设计了如下方案(尾气处理装置未画出)。
(1)如下图所示,通入干燥的Cl2后,同学们发现甲中红色布条不褪色,乙中红色布条褪色了,此实验中控制的变量是_________,该实验中发生了“Cl2+H2O=HCl+HClO”反应,若要说明HClO具有漂白性,需要补充的实验是__________。将乙中的布条取出烘干,发现未变为原来的红色,说明HClO漂白性是_______(填“可恢复的”或“不可恢复的”)。
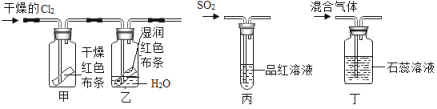
(2)如图丙所示,向品红溶液中通停止通气体,加热试管,发现试液又变为红色,说明SO2漂白的反应原理与Cl2漂白的反应原理是_____________(填“相同的”或“不同的”)
(3)如图丁所示,将干燥的Cl2和SO2按分子数之比1:1混合,通入石蕊试液中,发现石蕊试液变红,却不褪色。试用化学反应方程式作出解释(已知:生成物中氯元素显-1价,硫元素显+6价):__________。
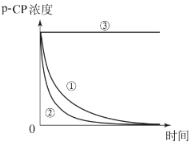
Ⅱ Fenton法常用于处理含难降解有机物的工业废水,其原理是利用Fe2+和H2O2的反应产生能降解污染物的活性成分,现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或者40℃(其余实验条件见下表),设计如下对比试验。
(1) 请完成以下实验设计表(表中不要留空格)
实验编号 | 实验目的 | 温度 ℃ | pH | 浓度/(mgL-1) | |
H2O2 | Fe2+ | ||||
① | 为②③提供参照 | 25 | 3 | 204 | 16.8 |
② | 探究温度对降解反应速率的影响 | ___ | ___ | 204 | 16.8 |
③ | _____________________________ | 25 | 10 | 204 | 16.8 |