题目内容
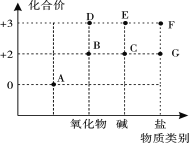
【题目】从化合价和物质类别两个维度认识元素及其化合物性质是重要的化学学习方式。下图是Fe及其化合物的化合价——物质类别二维图。
(知识卡片):
在化学反应中有元素化合价升高,则必有元素化合价降低,且化合价升高的总数一定等于化合价降低的总数。
请回答下列问题:
(1)A物质所属物质类别是_____。
(2)B的化学式是_____。
(3)工业上可以用_____(填物质名称)和D在高温下反应生产A。
(4)G可以是硫酸盐,这种硫酸盐可用作_____病人的治疗药物之一、
(5)C在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式是_____。
(6)高铁酸钾(K2FeO4)是常用的自来水消毒剂,高铁酸钾中铁的化合价为_____。
【答案】单质 FeO 一氧化碳 贫血 4Fe(OH)2+O2+2H2O=4Fe(OH)3 +6
【解析】
(1)A物质中,铁元素的化合价为0,所以该物质是单质;故填:单质;
(2)B是一种氧化物,其中铁元素显+2价,所以该物质是氧化亚铁,其化学式为FeO;故填:FeO;
(3)D是一种氧化物,其中铁元素显+3价,所以D物质是氧化铁,一氧化碳具有还原性,在工业上可用一氧化碳和氧化铁在高温的条件下制备金属铁;故填:一氧化碳;
(4)G是一种盐,其中铁元素显+2价,若是硫酸盐,则该物质就是硫酸亚铁,可为人体补充铁元素,治疗贫血;故填:贫血;
(5)C、E都是碱,C中,铁元素显+2价,E中,铁元素显+3价,因为氢氧根显-1价,所以C的化学式为Fe(OH)2,E的化学式为Fe(OH)3,氢氧化亚铁在潮湿的空气中与氧气、水发生化合反应生成氢氧化铁;故填:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(6)因为钾元素显+1价,氧元素显-2价,则设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价。故填:+6。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案