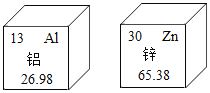
题目内容
【题目】设计对比实验是实验探究的重要方法。
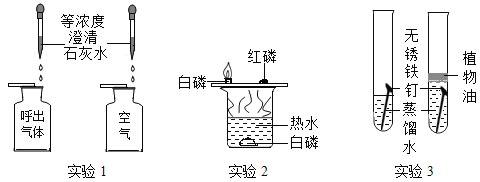
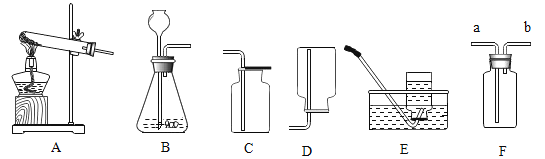
(1)实验1:探究人体呼出气体中二氧化碳含量比空气中的高,除了要控制两个盛装气体样品的集气瓶大小规格相同外, 还要控制________相同。
(2)实验2:通过观察_______的现象说明可燃物燃烧条件之一是需要与氧气接触。
(3)实验3:要探究铁生锈的条件,还应该补充的实验是_______。
【答案】加入澄清石灰水的量 铜片上的白磷燃烧,水中白磷不燃烧 取一个洁净试管,加入铁钉,通入干燥空气后密封试管
【解析】
(1)对比实验中变量是唯一的,题目中已知二氧化碳浓度不同,所以变量已经确定,则其他实验条件需要一致,在集气瓶大小规格相同外,还应保证加入试剂的量相同,即加入澄清石灰水的量相同;
(2)影响因素为氧气,则其他条件一致,所以选择相同的可燃物,相同温度,而一个可燃物与氧气,一个可燃物与氧气隔绝,达到实验的目的,所以观察到铜片上的白磷燃烧,水中白磷不燃烧,可以说明燃烧需要与氧气接触;
(3)铁生锈需要同时接触氧气和水,图中实验变量为氧气,所以还需要增加一个实验,与第一个试管内实验组成对比实验,验证水是铁生锈的条件之一,因此可以取一个洁净试管,加入铁钉,通入干燥空气后密封试管,从而与第一个试管组成对照实验,将水作为变量,进行铁生锈条件的探究。

 53随堂测系列答案
53随堂测系列答案【题目】皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
(提出问题)(1)白色沉淀A是什么?
(2)无色滤液B中的溶质有哪些?
(查阅资料)腌制皮蛋的原料配方是少量NaCl、CaO和Na2CO3过量的固体混合物。
(理论推理)(1)白色沉淀A是CaCO3,请写出生成该沉淀的化学方程式______。
(2)滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
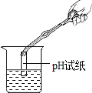
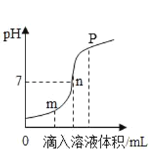
(实验验证)为证明滤液B中存在的三种溶质,同学们进行了如下实验。
步骤 | 实验操作 | 实验现象 | 实验结论 |
I | 取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤 | ______ | 滤液B中含有Na2CO3、NaOH、NaCl |
II | 取少量步骤I中所得滤液于试管中,加入酚酞溶液 | ______ | |
III | 另取少量步骤I中所得滤液于试管中,先加入足量的稀硫酸,再加入______溶液 | 产生白色沉淀 |
(拓展提升)
(1)向步骤I中加入过量Ba(NO3)2溶液的目的是______。
(2)小妮同学认为若将步骤I中的Ba(NO3)2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理______(填“合理”或“不合理”)。
(3)小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由______。
【题目】下表列出了1 ~18号元素的原子序数和元素符号:
原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
元素符号 | H | He | Li | Be | B | C | N | O | F |
原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
请回答下列问题:
(1)1 ~18号元素中属于稀有气体元素的有He、Ne、_____________ (填元素符号)。
(2)1 ~18号元素中最外层有2个电子的原子有____________、Be、Mg(填元素符号)。
(3)某元素的原子结构示意图为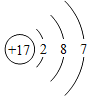 ,它在化学反应中一般易______________电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为_______________;它与11号元素组成的物质是由__________;构成的(填“分子”、“原子”或“离子”)。
,它在化学反应中一般易______________电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为_______________;它与11号元素组成的物质是由__________;构成的(填“分子”、“原子”或“离子”)。
(4)科学家已经研究出7号元素对应的高能微粒N5+,每个N5+中含有______________个质子和____________个电子。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是____________(单选,填字母序号)
A NO和O2
B CO和N2
C SO2和CO2
D SO2和SO3
【题目】化学实验技能是学习化学和进行探究活动的基础和保证。以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:_____。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
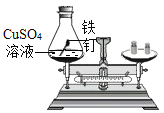
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液由蓝色变为浅绿色,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确,反应的化学方程式:_____ |
(反思与评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____中进行。
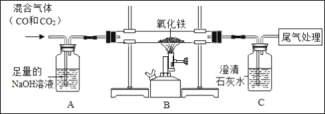
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是_____。
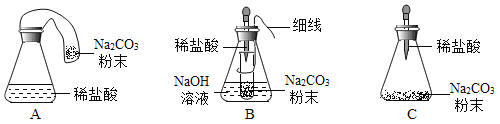
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。