题目内容
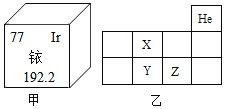
【题目】生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2会越来越多,因此将CO2转化为O2,不仅有科学意义也有重要的实用价值。据科学文献报道,NiFe2O4在一定条件下既能促进CO2分解又可重复使用。NiFe2O4在此反应中是( )
A. 粘合剂B. 制冷剂C. 防腐剂D. 催化剂
【答案】D
【解析】
NiFe2O4在一定条件下既能促进CO2分解又可重复使用,说明NiFe2O4是将二氧化碳转化为氧气,而没有和二氧化碳反应,故NiFe2O4不是反应物,NiFe2O4起到催化剂的作用,是催化剂。
A、![]() 在该过程中作催化剂,不是粘合剂,故A不正确;
在该过程中作催化剂,不是粘合剂,故A不正确;
B、![]() 在该过程中作催化剂,不是制冷剂,故B不正确;
在该过程中作催化剂,不是制冷剂,故B不正确;
C、![]() 在该过程中作催化剂,不是防腐剂,故C不正确;
在该过程中作催化剂,不是防腐剂,故C不正确;
D、![]() 在该过程中作催化剂,故D正确。故选D。
在该过程中作催化剂,故D正确。故选D。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
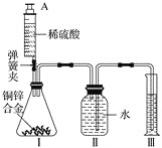
金博士一点全通系列答案【题目】化工生产中的废弃物再利用,可以有效节约资源、保护环境,下图是某化工厂利用废硫酸制备K2SO4的工艺流程图:
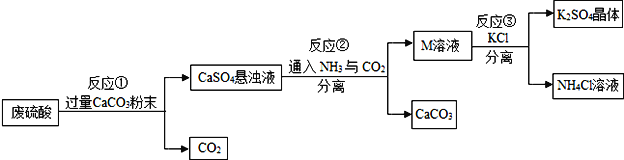
(1)生产上将CaCO3研成粉末的目的是______;
(2)写出反应![]() 的化学方程式______;
的化学方程式______;
(3)反应②充分反应后物质分离的方法是______;
(4)上述流程中,M溶液中溶质的主要成分是______(填写化学式);
(5)分析下表所示数据,则反应③在常温下可实现的原因是______;
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(6)洗涤反应③所得晶体最适宜的试剂是______(填序号);
AH2O B饱和K2SO4溶液 C 不饱和K2SO4溶液 D三者均可
(7)检验K2SO4晶体是否洗涤干净的方法是________________________________________。
(8)取50t质量分数为9.8%废硫酸用于该工艺制备K2SO4,理论可得到K2SO4质量为____t。
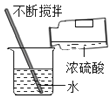
【题目】某化学兴趣小组利用稀盐酸和澄清石灰水展开“酸碱中和反应”的实验探究活动。请你参与他们的实验活动,并回答相关问题
(提出问题Ⅰ)稀盐酸和澄清石灰水能否发生反应?
(实验1)小明取一定量的稀盐酸,测得其pH=2,然后向其中加入一定量的澄清石灰水后,测得混合溶液的pH=3,于是得出“稀盐酸和澄清石灰水发生了中和反应”的结论。
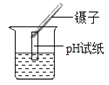
测定溶液pH的方法是:将pH试纸放在玻璃片上,___,将试纸显示的颜色与标准比色卡比较。
小刚认为,小明的实验方案不能证明二者发生了中和反应,理由是___。
(实验2)小刚取稀盐酸于试管中,加入一定量的澄清石灰水,得到溶液X,再加入适量铁粉,观察到___,证明稀盐酸和澄清石灰水发生了反应。
稀盐酸和澄清石灰水反应的化学方程式为___。
(提出问题Ⅱ)溶液X中溶质的成分是什么?
猜想一:只有CaCl2;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和HCl
小组同学为验证猜想二,进行了如下实验(查阅资料显示CaCl2溶液显中性)
实验操作 | 实验现象 | 实验结论 | |
实验3 | 取适量溶液X于试管中,滴加紫色石蕊溶液 | ___ | 猜想二成立 |
实验4 | 取适量溶液X于试管中,滴加Na2CO3溶液 | 产生白色沉淀 | 猜想二成立 |
小明认为实验4中产生白色沉淀,并不能证明猜想二成立,理由是____。
请你另选一种试剂,设计合理的方案,当观察到与实验4相同的现象时,证明猜想二成立。你的实验原理是___(用化学方程式表示)。