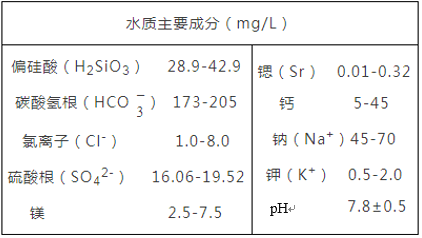
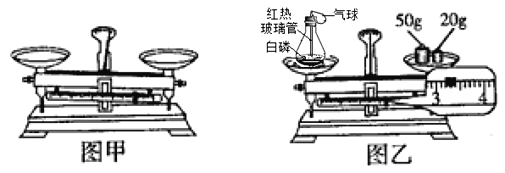
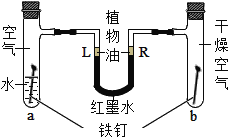
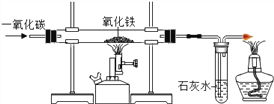
题目内容
【题目】化学课外小组同学取8g石灰石(主要成分是CaC03)样品于烧杯中,进行测定实验。现将40g稀盐酸 分四次加入烧杯中(反应的化学方程式为:CaC03+2HCl=CaCl2+C02↑+H20,石灰石中其他杂质不溶于水也不参与反应,反应生成的CaCl2能全部溶解在水中),充分反应后,测得有关数据如下表所示:
实验 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸的质量/g | 10 | 10 | 10 | 10 |
烧杯中剩余固体的质量/g | 5.5 | 3.0 | m | 1.2 |
(1)8g石灰石样品中杂质的质量为__________g;
(2)上表中m的数值是____________;
(3)高温锻烧石灰石样品可制得生石灰(CaO)和二氧化碳。如果锻烧这种石灰石样品100kg(杂质不反应),理论上最多能制得氧化钙多少____________kg?(根据化学方程式列式计算,注意格式的规范)
【答案】1.2 1.2 47.6g(详见解析)
【解析】
第一次加入10g盐酸,固体减少2.5g,可以猜测每10g盐酸能消耗碳酸钙2.5g,则第二次加入后固体剩余3g,又消耗碳酸钙2.5g,若固体碳酸钙足量,第三次应剩余0.5g,第四次加入还剩余1.2g说明第三次已将石灰石中碳酸钙完全消耗,也就确定m就应该为1.2g。最后1.2g应该为不能反应的杂质。
根据以上分析可知:
(1)8g石灰石样品中杂质的质量为1.2g;
(2)上表中 m 的数值是1.2g;
(3)碳酸钙的总质量为8g-1.2g=6.8g,样品中碳酸钙的质量分数=![]() ,100kg中碳酸钙的质量=100kg×85%=85kg。
,100kg中碳酸钙的质量=100kg×85%=85kg。
设:85kg 的碳酸钙分解生成氧化钙的质量为x。

![]() x=47.6kg
x=47.6kg
答:如果锻烧这种石灰石样品 100kg(杂质不反应),理论上最多能制得氧化钙47.6kg。

【题目】有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。课外小组为了测定该石灰石样品中碳酸钙的质量分数,将一定量的石灰石样品放入烧杯中,再将100 g稀盐酸分4次加入烧杯中,每次均充分反应。实验数据记录如下:
次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
反应后烧杯中物质的总质量/g | 35.2 | 58.4 | 82.6 | 107.6 |
(1)第1次加入稀盐酸充分反应后,生成二氧化碳的质量。
(2)该石灰石样品中碳酸钙的质量。