题目内容
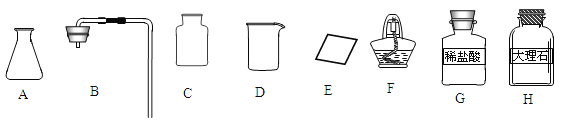
【题目】(7分)FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
写出本实验发生反应的化学方程式 .
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到 ,就可以粗略判断,得出实验结果.

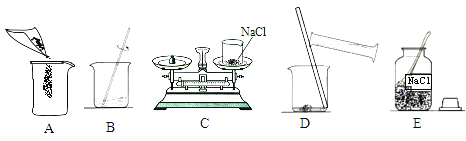
为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
Ⅱ.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定 ;
方案二的实验测量结果:
| 30% H2O2溶液的体积(mL) | 2% FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
1 | 5 | x | 20 | 5 | V1 |
2 | 10 | 3 | 15 | y | V2 |
表中x= ,y= .
实验结论:通过测量,若V1 V2(填“>”、“=”或“<”),说明 .
【答案】2H2O2 FeCl3 2H2O+O2↑ Ⅰ、水槽中产生气泡的速率和量筒内水的下降速率
Ⅱ、[方案二] 相同时间收集气体的体积 3 5 <
在不同过氧化氢浓度下,相同时间收集气体的体积不同
【解析】
试题分析:过氧化氢溶液在FeCl3溶液的催化下发生反应的化学方程式:2H2O2 FeCl3 2H2O+O2↑
Ⅰ、为探究过氧化氢浓度对过氧化氢分解速率的影响:分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,观察到水槽中产生气泡的速率和量筒内水的下降速率,就可以粗略判断,得出实验结果
Ⅱ、[方案二] 在不同过氧化氢浓度下,测定相同时间收集气体的体积;在实验中要注意控制变量,所以 根据实验2中的数据,故表中x=3;因为是探究[方案二]即测相同时间收集气体的体积,故表中y=5; 通过测量,若V1<V2,说明:过氧化氢浓度越大,相同时间收集气体的体积越多(或过氧化氢溶液分解速率就越快)

 阅读快车系列答案
阅读快车系列答案