题目内容
【题目】请认真回忆物质与其构成粒子之间的关系,回答下列问题:
(1)金属铁是由 构成的,氯化钠是由 构成的,二氧化碳是由 构成的。(填 “原子”、“分子”或 “离子”)
(2)原子得到或失去电子后形成离子。某粒子的结构示意图为
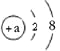
①当a= 时,该粒子是原子,该原子位于元素周期表中第 周期。
②当a=8时,该粒子是 (填“原子”、“阳离子”或 “阴离子”)。
【答案】原子 离子 分子 10 二 阴离子
【解析】
(1)构成物质的微粒:分子、原子、离子,由分子直接构成的物质:非金属气体单质、酸和多数氧化物;由原子直接构成的物质:金属、稀有气体、固态非金属等;由离子直接构成的物质有含有金属的混合物;故金属铁是由原子构成的,氯化钠是由离子构成的,二氧化碳是由分子构成的。
(2)①在原子中,质子数=核外电子数,故当a=2+8=10时,该粒子是原子,此时核外电子排布的电子层数=周期数,故该原子位于元素周期表中第二周期;②当质子数a=8<核外电子数是10,该粒子,带上了负电荷,成为阴离子。

【题目】化学老师交给某学校研究性学习小组一个任务:测定实验室里一瓶久置的![]() 固体是否变质.该小组的同学进行了如下实验探究:
固体是否变质.该小组的同学进行了如下实验探究:
提出问题:猜想![]() :没变质,全部是
:没变质,全部是![]() ;
;
猜想![]() :部分变质,________;
:部分变质,________;
猜想![]() :完全变质,全部是
:完全变质,全部是![]() .
.
查阅资料:部分溶液在常温下的![]() 如下:
如下:
盐溶液 |
|
|
|
| 等于 | 大于 | 等于 |
设计方案并进行实验:请你与他们一起共同完成,并回答所给问题.
实验步骤 | 实验现象 | 实验结论 |
①称取上述氢氧化钠固体样品 | 产生白色沉淀 | 说明久置固体中,一定含有 ________(填化学式). |
②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块 |
| 说明久置固体中,还一定含有 ________ (填化学式). |
上述步骤①中,称量氢氧化钠固体样品用到的玻璃仪器名称是________,滴加过量![]() 溶液的目的是________
溶液的目的是________
实验结论:通过实验,说明上述猜想中________是正确的.
拓展:该小组同学为测定出该![]() 固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为
固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为![]() ,则原样品中
,则原样品中![]() 的质量分数为________ (保留一位小数).
的质量分数为________ (保留一位小数).
反思:久置的氢氧化钠变质的原因是________(用化学方程式表示).