��Ŀ����
����Ŀ���������̨�ٰ����3.15�����ᣬ�س�ijƷ�ƽ���Ʒ�����¼�������ͬѧ�ǵĺ��档ij��ѧ��ȤС������ʦ�İ����£��Լ��ֳ���������Ʒ�����Ľ�����������ص�̽�����
��������⣩
��1������������ٻƽ�
��2������ȷ���ٵĽ�����ԣ�
���������ϣ�
��1���ٻƽ�ͨ���ǻ�ͭ��Cu��Zn�Ͻ𣩣�
��2���٣�Pd��������ɫ���н�������������Ʒ��
��ʵ��ҩƷ���١�����Pt����ϡ���ᡢ��������Һ���Ȼ��٣�PdCl2����Һ
��ʵ��̽����
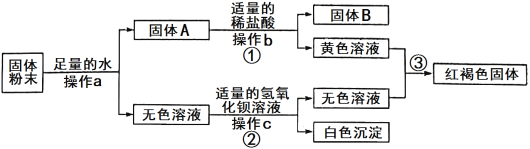
��1������ƽ���Ʒ�����ȡ�ƽ���Ʒ���Թ��У��μ�ϡ����۲쵽�ƽ���Ʒ���������ݲ�������������_____��д���÷�Ӧ�Ļ�ѧ����ʽ______��˵������ƷΪ______��ѡ�������������������ƽ�
��2��̽���ٵĽ��������������飬ͬѧ�Dz����ٵĻ�Կ��������Ͳ����������������������ҩƷ��������ʵ�飺
ʵ�鲽�� | ʵ������ | ʵ����� |
���ٽ�����������Һ�� | _____�� | �ٵĻ�Ա����� |
�Ѳ������Ȼ�����Һ�� | ���������� | �ٵĻ�ԱȲ�_____ |
�����ó����ۣ��١��������Ľ��������ǿ������˳��Ϊ________________��
����Һ������
��1��ת���ɳ�����С��ͬѧ������Һ�嵹���Һ���У������Ȼ����İ�ɫ������д�������ó����Ļ�ѧ����ʽ_______________________��
��2��ͨ����ѧ�����ķ�����һ�����ս����١�
���𰸡�H2 Zn+2HCl=ZnCl2+H2�� �� ���������� ǿ �����١��� PdCl2+2AgNO3=2AgCl��+Pd��NO3��2
��������
[ʵ��̽��]
��1��ȡ�ƽ���Ʒ���Թ��У��μ�ϡ����۲쵽�ƽ���Ʒ���������ݲ��������������������������������Ʒ�е�п��Ӧ�����Ȼ�п����������Ӧ�Ļ�ѧ����ʽΪZn+2HCl=ZnCl2+H2����˵������ƷΪ�ٻƽ�
��2��ʵ��̽���ٵĽ�����ԣ����ٽ�����������Һ�У��Ƚ��ٺ����Ļ����ԣ���ʵ��ó��������ٵĻ�Ա����������ʵ�����������Ѳ������Ȼ�����Һ�У��۲쵽���������������û��٣��ٵĻ�ԱȲ���ǿ��
�ó����ۣ��١��������Ľ��������ǿ������˳��Ϊ�����١�����
[��Һ����]
��1��ת���ɳ�����������Һ�嵹���Һ���У������Ȼ����İ�ɫ����������Ϊ�Ȼ��ٺ���������Ӧ�����Ȼ����������٣���ѧ����ʽΪ![]() ��
��