题目内容
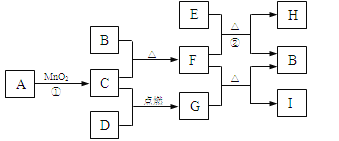
【题目】(10分)A~I为初中化学常见的物质,它们之间的转化关系下图所示(只略去反应①的部分产物)。其中B是紫红色金属;D、F为黑色固体;H是实验室中最常见的无色无味液体。请回答:
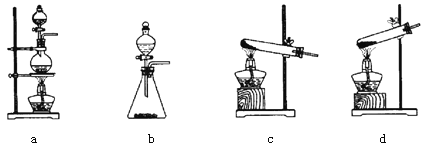
(1)若A在常温下为固体,则反应①的化学方程式为 ,下图所示的仪器中,可用作该反应发生装置的是 (填字母);若A在常温下为液体,则A的化学式为 ,反应①的基本反应类型是 。
(2)在金属活动性顺序中,B位于铁的 (填“前面”或“后面”)。若要证明,所需试剂有:B的单质、铁的单质和 (只填一种)。
(3)G的化学式为 ,它不具有的性质有 (填字母)。
A.酸性 B.还原性 C.毒性 D.助燃性
(4)反应②的化学方程式为 。
【答案】(1)2KClO3![]() 2KCl + 3O2↑ c H2O2 分解反应
2KCl + 3O2↑ c H2O2 分解反应
(2)后面 盐酸或稀硫酸、铜盐、亚铁盐等
(3)CO A、D
(4)![]()
【解析】
试题分析:(1)A在二氧化锰的催化作用下反应,若A是固体,那么A是氯酸钾,氯酸钾分解生成氯化钾和氧气;B是紫红色金属,那么B是铜;C与B在加热的条件下反应,故C是氧气,铜与氧气反应生成黑色的氧化铜,即F是氧化铜;D是黑色固体,D能与氧气再点燃的条件下反应,还能与氧化铜反应,故D是碳,碳和氧气反应生成一氧化碳,一氧化碳还原氧化铜生成二氧化碳,即G是一氧化碳,那么I是二氧化碳;H是实验室中最常见的无色无味液体,那么H是水。E和氧化铜反应得到了铜和水,故E是氢气。把推断出的物质带入,推断正确。
实验室用加热氯酸钾的方法制取氧气,选固固加热型,即选c装置;若A是液体,那么A是过氧化氢,过氧化氢分解生成水和氧气,属分解反应;
(2)B是铜,铜位于铁的后面;要证明铜和铁的金属活动性可用稀盐酸或稀硫酸;
(3)G是一氧化碳,一氧化碳具有可燃性、还原性和毒性;
(4)反应2是氢气还原氧化铜,生成的是铜和水:![]() 。
。

【题目】下列实验方法一定能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
B | 鉴别 | 分别点燃,在火焰上方罩一干冷烧杯 |
C | 鉴别石灰水和 | 加入适量的稀盐酸 |
D | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入 |