题目内容
【题目】实验室常用下列装置制取气体,请你根据所学知识回答下列问题.
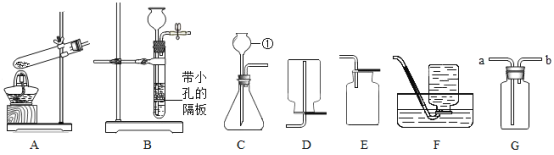
(1)写出编号所指仪器的名称:①_____;
(2)装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列橫线上:①_____;②_____;上述装置改进后,请继续回答下列问题.
(3)用高锰酸钾制取比较纯净的氧气应选择上述装置中的A和_____(填字母),写出该反应的化学方程式:_____;此反应类型是_____.
(4)实验室选用C和E装置组合制取二氧化碳气体,还可以选择上述装置中的(填字母)_____代替C;该反应的化学方程式:_____;
(5)比较B、C装置的不同,指出B装置的优点是_____;
(6)有一名同学欲用G装置收集H2,则H2应从导管口_____通入.(填写a或b)
【答案】长颈漏斗 A中试管口应该略向下倾斜 E中导管应该伸入集气瓶的底部 F 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 可以随时控制反应的发生和停止 b
K2MnO4+MnO2+O2↑ 分解反应 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 可以随时控制反应的发生和停止 b
【解析】
(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)装置图中共有两处明显的错误,改正结果是:A中试管口应该略向下倾斜;E中导管应该伸入集气瓶的底部;故答案为:A中试管口应该略向下倾斜;E中导管应该伸入集气瓶的底部;
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平,属于分解反应;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:F;2KMnO4![]() K2MnO4+MnO2+O2↑;分解反应;
K2MnO4+MnO2+O2↑;分解反应;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(5)B装置的优点是:可以随时控制反应的发生和停止;故答案为:可以随时控制反应的发生和停止;
(6)用G装置收集H2,则H2应从导管口b通入,因为氢气的密度比空气小;故答案为:b;

 初中学业考试导与练系列答案
初中学业考试导与练系列答案