题目内容
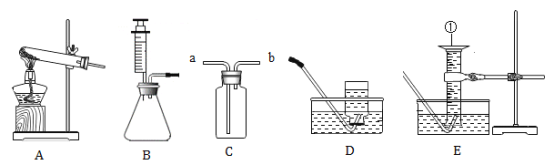
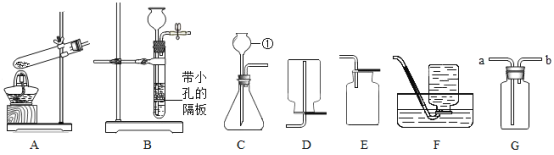
【题目】根据下列实验装置图回答问题:
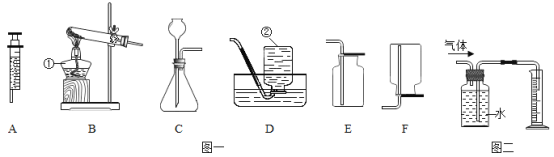
(1)写出图中编号仪器的名称:①_______,②_______
(2)实验室用氯酸钾和二氧化锰粉末制取较纯净的氧气应选用(图一中)的实验装置为___(填字母序号),写出该反应的文字表达式________________,反应的基本类型为_______
(3)组装发生装置B时,下列仪器用品的组装正确顺序是:铁架台→木块→___→___(填写序号) ①试管 ②酒精灯
(4)注射器A可用于检查装置C的气密性,步骤如下:
Ⅰ、向锥形瓶中加入少量水至___
Ⅱ、将注射器A连接到装置C的导管口处,推或拉注射器活塞,若看见___(填字母)时,则说明C装置气密性良好
A 拉活塞时锥形瓶中液面上升
B 推活塞时长颈漏斗中的液面低于锥形瓶内液面
C 拉活塞时长颈漏斗下端口有气泡冒出
D 推活塞时长颈漏斗中液面上升,并形成稳定水柱
⑤实验室用装置C制取CO2,如用注射器A替换长颈漏斗,其优点是____________
⑥图2装置的作用是_______________,集气瓶中水上方留有的空气对实验结果______(填“有”或“没有”)明显影响。
【答案】酒精灯 集气瓶 BD ![]() 分解反应 ② ① 没过长颈漏斗下端 CD 控制反应的速率 用来收集并测量生成的气体体积 没有
分解反应 ② ① 没过长颈漏斗下端 CD 控制反应的速率 用来收集并测量生成的气体体积 没有
【解析】
(1)酒精灯是常用的加热仪器,集气瓶是收集气体的仪器,故答案为:酒精灯;集气瓶;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,属于分解反应;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:BD;![]() ;分解反应;
;分解反应;
(3)组装发生装置B时,下列仪器用品的组装正确顺序是:铁架台→木块→酒精灯→试管;是按照由下到上的顺序,故答案为:②①;
(4)向锥形瓶中加入少量水至浸没长颈漏斗下端,将注射器A连接到装置C的导管口处,推或拉注射器活塞,若看见:拉活塞时长颈漏斗下端口有气泡冒出、推活塞时长颈漏斗中液面上升,并形成稳定水柱时,则说明C装置气密性良好;故答案为:浸没长颈漏斗下端;CD;
(5)用注射器替换长颈漏斗,其优点是:控制反应的速率,故答案为:控制反应的速率;
(6)图2装置的作用是:用来收集并测量生成的气体体积,集气瓶中水上方留有的空气对实验结果没有明显影响,故答案为:用来收集并测量生成的气体体积;没有.

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】做完“铁在氧气里燃烧”实验后,小明同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与.
(问题)铁燃烧时溅落下来的黑色物质中还有没有铁呢?
(查阅资料)(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3)
(2)铁的氧化物均能溶于酸的溶液.
(实验探究)将冷却后的黑色物质碾碎,装入试管,加入 ______ 溶液,观察到的现象是 ______,说明铁燃烧时溅落下来的黑色物质中还含有铁.
(问题)铁燃烧的产物为什么不是 Fe2O3呢?
(查阅资料)
(1)Fe3O4和Fe2O3分解温度、铁的熔点见表:
Fe3O4 | Fe2O3 | 铁 | |
分解温度/℃ | 1538 | 1400 |
|
熔点/℃ |
|
| 1535 |
(2)Fe2O3高温时分解成Fe3O4
(理论探讨)根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在 ______ 之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
(拓展研究)
(1)实验中为了防止集气瓶炸裂,必须 ______.
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式 ______.
(3)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色______,就说明包装盒破损进气,这样售货员就能及时发现并处理.
【题目】某物质在不同温度时的溶解度如下表所示。80℃时,该物质溶解于 100g 水形成 30%的溶 液。下列关于该溶液的说法正确的是( )
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
A. 溶质可能为 Ca(OH)2B. 含有 169g 的溶质
C. 溶液达到饱和状态D. 降温至 20℃~40℃时,有晶体析出
【题目】化学反应条件的控制是实验的灵魂”.某探究小组发现若反应过快,产生的气体不易及时收集,为探究影响过氧化氢溶液分解快慢的因素,于是进行了如下探究:
(提出问题)过氧化氢溶液分解快慢与哪些因素有关呢?
(猜想与假设)猜想一:可能与过氧化氢的质量分数有关;
猜想二:可能与____有关;
猜想三:可能与是否用催化剂有关.
(设计并实验)该探究小组用不同质量分数的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧气体积和反应所需时间,记录数据如表.
实验 序号 | 过氧化氢的 质量分数 | 过氧化氢溶液 体积(mL) | 温度 | 二氧化锰 的用量/g | 收集氧气 的体积/ml | 反应所需 的时间/s |
① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30% | 5 | 35 | 2 | 49.21 | |
④ | 30% | 5 | 55 | 2 | 10.76 |
(收集证据)要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是_____(选填“实验序号”).由实验③和④对比可知,化学反应速率与温度的关系是:________./span>
(解释与结论)
(1)通过探究,了解控制过氧化氢分解快慢的方法.请写出过氧化氢溶液在二氧化锰的催化作用下生成氧气的文字表达式为:_____________.
(2)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量_________.(填“减小”、“增大”或“不变”)