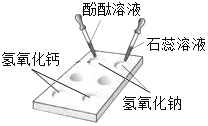
题目内容
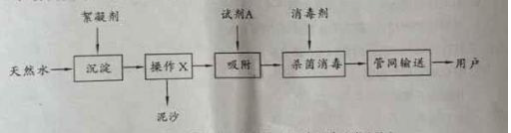
【题目】为除去粗盐中含有的硫酸钠、氯化镁、氯化钙等杂质,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质将杂质转化为沉淀过滤除去,再向滤液中加入适量的盐酸得到精盐水。该过程示意如图:
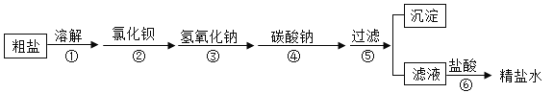
对该过程的认识中,正确的是( )
A.①操作中需要进行搅拌,目的是提高氯化钠的溶解度
B.②、④两步操作顺序可以颠倒
C.⑤操作得的沉淀中共有三种物质
D.⑥操作中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
【答案】D
【解析】
A、①操作中需要进行搅拌,目的是加快粗盐的溶解,并不能提高氯化钠的溶解度,A不正确;
B. ②、④两步操作顺序不可以颠倒,加入碳酸钠的目的是既可以除去氯化钙,又可以除去加入过量的氯化钡,如果②、④两步操作顺序颠倒,就会引进氯化钡杂质,所以加入碳酸钠的顺序一定要在加氯化钡后面,B不正确;
C、⑤操作得的沉淀中共有硫酸钡、氢氧化镁、碳酸钙和碳酸钡四种物质,C不正确;
D、⑥操作中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7,D正确。故选D。

 阅读快车系列答案
阅读快车系列答案【题目】如图所示装置可用于实验室制取某些气体,并能随开随用。下表中所选用的药品及制取的气体完全正确的一组是( )
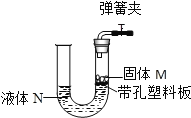
选项 | 选用药品 | 制取的气体 | |
固体M | 液体N | ||
A | 锌粒 | 稀硫酸 | 氢气 |
B | 碳酸钠 | 浓盐酸 | 二氧化碳 |
C | 大理石 | 稀盐酸 | 二氧化碳 |
D | 二氧化锰 | 过氧化氢 | 氧气 |
A.AB.BC.CD.D
【题目】现实验室中有一包由碳酸钠和氧化钙组成的白色粉末,下面是某化学兴趣小组的同学进行的探究过程,请你按要求帮助完成探究活动。
同学们将部分白色固体放于烧杯中加入少量的水,发现烧杯外壁有热感,加水放热的反应的化学方程式是_______________。继续加入足量的水并过滤,用pH试纸测定滤液的pH, pH_______________7 (选填“>、=、<”)。滤液呈碱性。
(提出问题)滤液中含有那些碱性物质?
(提出猜想)
猜想①: NaOH
猜想②: NaOH 和Na2CO3
猜想③: NaOH和Ca(OH)2
猜想④: NaOH、Ca(OH)2 和Na2CO3
[查阅资料] Na2CO3溶液呈碱性
(实验探究)
(1)甲同学认为猜想④不合理,原因是__________________(用化学方程式表示)。
(2)乙同学进行下列实验,请你填写表中空白处。
实验操作步骤 | 实验现象 | 结论 |
I.取用少量滤液于试管中,通入CO2 | 没有明显变化 | 滤液不含_________。 |
Ⅱ.取用少量滤液于试管中,滴加过量CaCl2溶液,后滴入无色酚酞试液 | ____________ | 滤液含有Na2CO3;反应的化学方程式是_____________。 |
_____________ | 滤液含有NaOH。 |
(获得结论)猜想②成立
(反思拓展)
实验操作步骤Ⅱ中加入过量CaCl2溶液的目的是__________________________。