题目内容
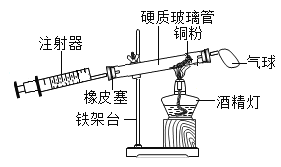
【题目】根据下图回答问题。
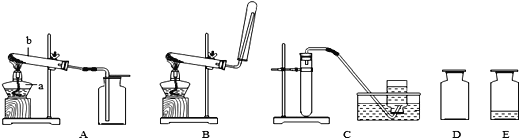
(1)写出标有序号仪器的名称:a_____
(2)实验室用高锰酸钾制取氧气应选用的装置是_______(填装置下方的字母序号),你认为该装置中还缺少_____,该化学反应的文字表达式为_________
(3)若用C装置制取氧气发生化学反应的文字表达式__________,反应的基本类型为_______。
(4)图中D、E是收集到的两瓶氧气,若进行硫磺在氧气中燃烧的实验,应选用的一瓶是_____(填装置下方的字母序号)。
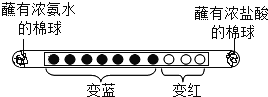
(5)氨气是一种极易溶于水且密度比空气小的气体,实验室常用加热氯化铵和氢氧化钙固体混合物来制取氨气。则实验室制取氨气应选择的装置是_______(填序号)。收集氨气只能选用向下排空气法,其原因是_____。
(6)下表是研究性学习小组研究影响过氧化氢分解速率的因素时采集的一组数据:用10mL过氧化氢溶液制取150mL氧气所需的时间(秒)
浓度 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
无催化剂、加热 | 360s | 480s | 540s | 720s |
MnO2催化剂、不加热 | 40s | 60s | 120s | 180s |
MnO2催化剂、加热 | 10s | 25s | 60s | 120s |
① 该研究小组在设计方案时,考虑了_______、_______、_______等因素对过氧化氢分解速率的影响.
② 从上表的数据中,你能得出什么结论?(填两点)
_________。、__________。
【答案】酒精灯 A 试管口放一团棉花 高锰酸钾 ![]() 锰酸钾+二氧化锰+氧气 过氧化氢
锰酸钾+二氧化锰+氧气 过氧化氢 ![]() 水+氧气 分解反应 E B 氨气极易溶于水且密度比空气小 浓度 温度 催化剂 浓度越高,过氧化氢的分解速率越快 温度越高,过氧化氢的分解速率越快
水+氧气 分解反应 E B 氨气极易溶于水且密度比空气小 浓度 温度 催化剂 浓度越高,过氧化氢的分解速率越快 温度越高,过氧化氢的分解速率越快
【解析】
(1)根据常见仪器的名称解答;
(2)根据用高锰酸钾制取氧气的反应的原理,反应物的状态和反应条件,氧气的性质,实验注意事项进行分析解答;
(3)根据用过氧化氢制氧气的原理进行分析解答;
(4)根据二氧化硫的性质进行分析解答;
(5)根据题中提供制氨气的反应物的状态和反应条件以及氨气的性质进行分析解答;
(6)根据实验中提供的数据进行分析解答。
(1)仪器a的名称是酒精灯;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气的密度小于空气,所以应选用的装置是A,防止高锰酸钾粉末进入导管,试管口放一团棉花,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾 ![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
(3)C装置制取氧气的反应物是固体和液体,反应条件是常温,所以试管中应盛放的药品是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰的催化作用下生成水和氧气,文字表达式为:过氧化氢 ![]() 水+氧气该反应;是由一种物质生成物两种物质,属于分解反应;
水+氧气该反应;是由一种物质生成物两种物质,属于分解反应;
(4)硫磺在氧气中燃烧生成二氧化硫,二氧化硫有毒,会污染空气,二氧化硫能溶于,集气瓶内放少量的水,能吸收二氧化硫,所以若进行硫磺在氧气中燃烧的实验,应选用的一瓶是E;
(5)实验室制取氨气的反应物是固体,反应条件是加热,氨气极易溶于水且密度比空气小,所以实验室制取氨气应选择的装置是B;氨气极易溶于水且密度比空气小,收集氨气只能选用向下排空气法;
(6)①通过表中数据可知,影响因素有浓度、温度和催化剂;
②通过表中数据可知,浓度越高,过氧化氢的分解速率越快(或温度越高,过氧化氢的分解速率越快;使用催化剂,过氧化氢的分解速率越快)。

 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】了解物质的结构,有利于理解和认识化学问题。
(1)下表为部分元素的原子结构示意图。
元素名称 | 氢 | 氦 | 氮 | 氧 | 钠 | 硫 |
元素符号 | H | He | N | O | Na | S |
原子结构 示意图 |
|
|
|
|
|
|
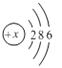
①表中硫原子的核电荷数x为__,硫原子得到两个电子所形成离子的符号为__。
②表中具有相对稳定结构的原子是__(填元素符号)。
③表中所列6种元素中,位于第三周期的非金属元素有__种。
④钠元素与硫元素可形成化合物硫化钠,该化合物的化学式为__。
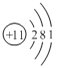
⑤氮元素在元素周期表中的信息如图所示,下列说法错误的是(________)
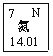
a.氮原子的质子数为7
b.氮元素的相对原子质量为14.01 g
c.氮原子最外层电子数为7
(2)汽车尾气净化装置中装有催化剂,尾气在催化剂表面反应的微观过程可用下图表示。
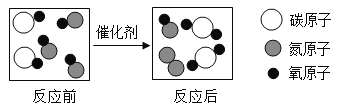
①该反应中涉及的氧化物共有____种。
②反应后生成的“![]() ”与“/span>
”与“/span>![]() ”对应物质的质量比为____。
”对应物质的质量比为____。