题目内容
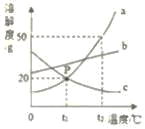
【题目】如图是a、b、c三种不含结晶水的固体物质的溶解度曲线,下列说法中正确的是( )
A. a的溶解度比c大
B. t1℃时,a的饱和溶液中溶质与溶液的质量比为1:5
C. 将t2℃a、b、c的三种饱和溶液分别降温至t1℃,所得溶液的溶质质量分数b>a>c
D. c可能为气体,它的饱和溶液变为不饱和溶液,可采用升温的方法
【答案】C
【解析】
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
A、在比较物质的溶解度时,需要指明温度,故A不正确;
B、t1℃时,a物质的溶解度是20g,所以a的饱和溶液中溶质与溶液的质量比为
![]() ,故B不正确;
,故B不正确;
C、t1℃时,b物质的溶解度最大,a、c物质的溶解度相等,降低温度,a、b物质的溶解度减小,c物质的溶解度增大,应该按照t2℃时的溶解度计算,所以将t2℃,a、b、c的三种饱和溶液分别降温至t1℃,所得溶液的溶质质量分数b>a>c,故C正确;
D、c可能为气体,它的饱和溶液变为不饱和溶液,可采用降温的方法,故D不正确。故选C。

 考前必练系列答案
考前必练系列答案【题目】某化学兴趣小组在探究氢氧化钠的化学性质时,做了如图一所示的 A、B、C 三个实验。
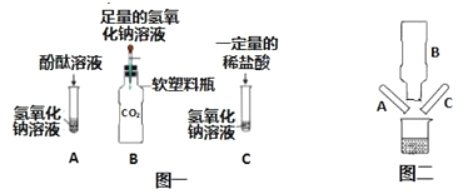
(1)写出实验B中反应的化学方程式_____。
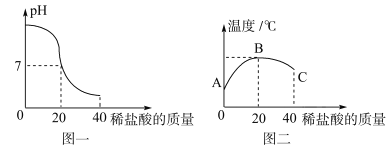
(2)实验结束后,小组同学将 A、B、C 三容器中的废液同时倒入一个洁净的烧杯中(如图二所示),产生_____现象,并最终得到无色溶液。同学们对所得溶液的溶质成分(不考虑指示剂)进行探究。
(查阅资料)初中常见物质溶液的pH
稀盐酸 | 氯化钠 | 碳酸钠 | 氢氧化钠 | |
溶液的 pH | <7 | =7 | >7 | >7 |
(提出猜想)甲同学猜想:溶液中溶质为 NaCl。
乙同学猜想:溶液中溶质为 NaCl、_____(填化学式,下同)。
(设计实验)设计实验证明猜想。
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,加入_____。 | 溶液变为蓝色。 | 乙同学的猜想成立。 |
(反思与总结)判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑_____。