题目内容
【题目】氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催化剂。以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:
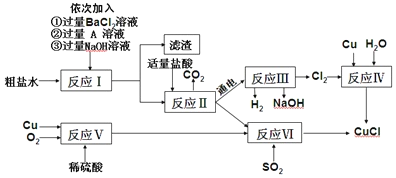
⑴A溶液中溶质的化学式是____________;
⑵写出反应III的化学方程式__________________________;
⑶反应VI的化学方程式是:2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4,反应中化合价升高的元素是_____________;
⑷本工艺中可循环利用的物质是NaOH和_____________;
⑸反应VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。真空干燥的目的是_____________________。
【答案】 Na2CO3 2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑ 硫 硫酸 防止氯化亚铜被氧化(加快乙醇和水的蒸发 ) 。
2NaOH+Cl2↑+H2↑ 硫 硫酸 防止氯化亚铜被氧化(加快乙醇和水的蒸发 ) 。
【解析】(1)加入氯化钡溶液可以除去硫酸根离子,加入碳酸钠溶液可以除去钙离子和过量的钡离子,加入氢氧化钠溶液可以除去镁离子,因此A溶液是碳酸钠溶液,碳酸钠的化学式是Na2CO3;(2)反应III中,电解饱和食盐水时,氯化钠和水反应生成氢氧化钠、氢气和氯气,反应的化学方程式为:2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑;(3)反应2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4中,氯化钠中钠元素的化合价是+1,氯元素的化合价都是1,硫酸铜中铜元素的化合价是+2,硫元素的化合价是+6,氧元素的化合价是2,二氧化硫中硫元素化合价是+4,氧元素化合价是2,水中氢元素化合价是+1,氧元素化合价是2,氯化亚铜中铜元素的化合价是+1,氯元素化合价是1,硫酸中氢元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,硫酸钠中钠元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,因此反应中化合价升高的元素是硫元素,由+4变成+6;(4)本工艺中可循环利用的物质是NaOH、H2SO4,电解生成的氢氧化钠可应用于反应Ⅰ,反应VI中生成的硫酸可应用于反应Ⅴ; (5)70℃真空干燥的目的是加快乙醇和水的蒸发,防止CuCl被空气氧化。
2NaOH+Cl2↑+H2↑;(3)反应2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4中,氯化钠中钠元素的化合价是+1,氯元素的化合价都是1,硫酸铜中铜元素的化合价是+2,硫元素的化合价是+6,氧元素的化合价是2,二氧化硫中硫元素化合价是+4,氧元素化合价是2,水中氢元素化合价是+1,氧元素化合价是2,氯化亚铜中铜元素的化合价是+1,氯元素化合价是1,硫酸中氢元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,硫酸钠中钠元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,因此反应中化合价升高的元素是硫元素,由+4变成+6;(4)本工艺中可循环利用的物质是NaOH、H2SO4,电解生成的氢氧化钠可应用于反应Ⅰ,反应VI中生成的硫酸可应用于反应Ⅴ; (5)70℃真空干燥的目的是加快乙醇和水的蒸发,防止CuCl被空气氧化。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
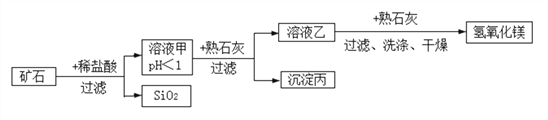
在溶液甲中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子逐步转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液乙的pH的取值有一定的范围。
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀的pH | 1.5 | 4.2 | 8.6 |
完全沉淀的pH | 3.2 | 6.7 | 11.1 |
下列说法错误的是
A. 溶液甲中共含有三种阳离子
B. 溶液乙的pH的范围是6.7<pH<8.6
C. 沉淀丙的成分是Fe(OH)3、Cu(OH)2、Mg(OH)2
D. 溶液乙中加入熟石灰发生的化学反应方程式:MgCl2+Ca(OH)2= Mg(OH)2↓+CaCl2
【题目】如图是某反应的微观示意图,下列有关说法正确的是( )

A. 反应前后分子的种类不变
B. 反应中生成的物质都是化合物
C. 该反应的基本类型属于复分解反应
D. 反应前后有三种元素的化合价均发生了变化
【题目】去年党的十九大会议使用了一种含碳酸钙的“石头纸”。为测定其中碳酸钙的含量,课外活动小组的同学共称取50g碎纸样品,分别放在5只烧杯中并编号,再分别向5只烧杯中加入浓度相同的稀盐酸进行实验。实验数据见下表(假设纸张中的其他成分既不溶于水,也不与盐酸反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | m | 3.52 |
(1)表中m的值为___________。
(2)求样品中碳酸钙的质量分数___________。
(3)求样品中碳酸钙和盐酸刚好完全反应后得到溶液溶质的质量分数(结果保留到小数点后第二位)___