题目内容
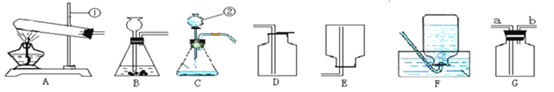
【题目】请结合下图回答问题:
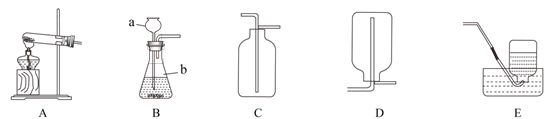
(1)标出仪器 a 的名称_____。
(2)实验室通常利用上图中_____装.置.的.组.合.制取二氧化碳(选填字母),该反应的化学方程式为_____________。
(3)选用 E 装置收集氧气的原因是_____。
(4)工业上煅烧石灰石可制得生石灰和二氧化碳。如果要制取 5.6t 氧化钙,理论上需要含 碳酸钙 80%的石灰石的质量是多少________?
【答案】 长颈漏斗; BC; CaCO3+2HCl=CaCl2+H2O+CO2↑; 氧气不易溶于水且不与水反应 12.5t
【解析】(1)图中标示a仪器的名称是长颈漏斗;(2)实验室制取二氧化碳气体时不需要加热,发生装置为B,二氧化碳密度比空气大,收集装置选C,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;(3)(3)选用 E 装置收集氧气的原因是氧气不易溶于水且不与水反应;(4)设需要含碳酸钙80%的石灰石的质量为![]() ,
,
CaCO3![]() CaO+CO2↑,
CaO+CO2↑,
10056
x×80%5.6t
![]()
![]() =12.5t。
=12.5t。

【题目】盐城的城市建设可谓是日新月异,在城市建设、生产、生活中材料有着广泛的应用。
(1)下列生活用品,主要利用金属具有良好导热性的是________(填序号),一般铜导线外面包有聚乙烯绝缘层,聚乙烯属于________材料。

(2)铁制品在空气中会发生锈蚀,其原因是铁与空气中的___________共同作用的结果。为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是_____________(要求一种方法即可)。
(3)化学小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如下实验方案:
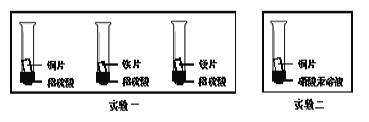
根据实验一判断出镁的金属活动性比铁强,依据的现象是___________;根据实验二的现象应得出的结论是__________。
(4)苗苗同学向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,充分反应后过滤,滤液呈浅绿色,再向滤液中放入一枚洁净的铁钉,足够时间后取出,铁钉表面无变化。根据此现象作出了下列判断,你认为正确的是_____________(填序号)。
A. 滤纸上一定有Fe,可能有Mg、Cu
B. 滤纸上一定有Cu,可能有Fe,一定没有Mg
C. 滤液中一定有FeSO4,可能有MgSO4 、CuSO4
D. 滤液中一定有MgSO4、FeSO4,一定没有CuSO4
(5)为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如表:
第I组 | 第Ⅱ组 | 第Ⅲ组 | |
稀硫酸的质量/g | 50 | 100 | 150 |
溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
根据实验及有关数据进行分析与计算:
①第I组实验中反应物___________(填“氧化铜“、“稀硫酸”或“氧化铜与稀硫酸”)反应完。
②20g样品中含氧化铜的质量分数分别为____________。
③计算所用的稀硫酸溶质的质量分数为____________(写出计算过程)
④将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。
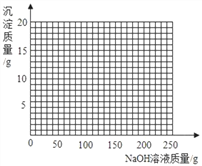 ___________________
___________________