题目内容
【题目】如图三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。
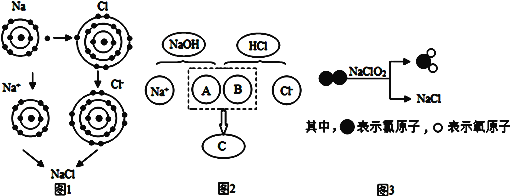
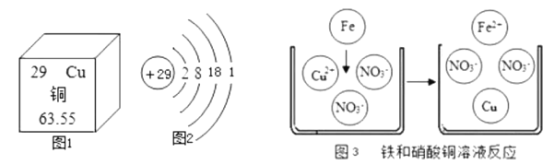
(1)如图是金属钠与氯气反应生成氯化钠的微观示意图。由如图可知,元素的化学性质与_____(填字母序号)有密切的关系。
A 电子层数 B 最外层电子数 C 核外电子数
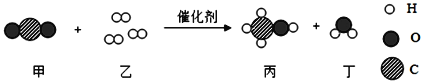
(2)如图中A、B处应填入的离子符号依次为_____、_____,该反应的实质为_____。
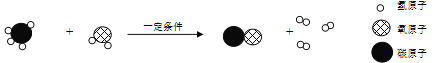
(3)如图所示反应的化学方程式为_____。
【答案】B OH- H+ H++OH-=H2O Cl2+2NaClO2=2NaCl+2ClO2
【解析】
(1)元素的化学性质于元素原子最外层电子数密切相关,故填:B;
(2)氢氧化钠与盐酸的反应生成了氯化钠和水,反应的方程式是:NaOH+HCl=NaCl+H2O;此反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子:H++OH-=H2O;氢氧化钠电离出A是氢氧根离子,盐酸电离出的B是氢离子,生成的C是水分子,所以A、B 处应填入的离子符号依次为 OH-、H+;酸碱中和反应的实质是氢离子和氢氧根离子反应生成水,故填:H++OH-=H2O。
(3)据图可以看出,该反应是 Cl2和NaClO2反应生成了ClO2和NaCl,则其化学方程式是:Cl2+2NaClO2=2NaCl+2ClO2。

【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如下:

(1)操作1把废渣粉碎的目的 。
(2)在废渣粉末中加入NaCl和O2的目的是:CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,写出该反应的化学方程式 。
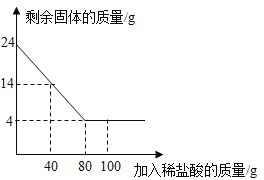
(3)【查阅资料】:不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.7 |
沉淀完全的pH | 3.2 | 6.7 |
操作3的名称是 ,其中用到玻璃棒的作用是 。在此操作之前,为了使溶液中的Fe3+变成Fe(OH)3沉淀而除去,你认为调节溶液的pH到 (填数值范围)比较合适。
(4)流程图中能循环利用的物质是 和水。