题目内容
某化学兴趣小组欲除去固体氯化钠中混有少量可溶性氯化镁和难溶性泥沙,设计如图所示实验方案,请参与实验并回答问题.
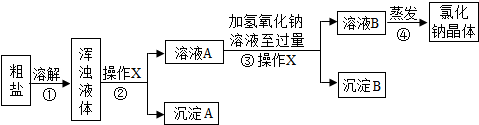
(1)步骤①中玻璃棒搅拌的作用是 .
(2)步骤②、③中,操作X的名称是 .
(3)步骤③中,加入过量氢氧化钠溶液的目的是 ;沉淀B的化学式是 .
(4)有同学认为原实验方案不完善,做出这种评价的依据是 .

(1)步骤①中玻璃棒搅拌的作用是
(2)步骤②、③中,操作X的名称是
(3)步骤③中,加入过量氢氧化钠溶液的目的是
(4)有同学认为原实验方案不完善,做出这种评价的依据是
考点:氯化钠与粗盐提纯,过滤的原理、方法及其应用,盐的化学性质
专题:常见的盐 化学肥料
分析:本题属于流程图型除杂质题,还包含了混合物分离中常用的方法,如过滤、蒸发等.一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.在本题中,加入的氢氧化钠溶液会与杂质氯化镁反应生成白色沉淀氢氧化镁.固体与液体分离要用过滤,要得到可溶性固体需要蒸发.由于加入的氢氧化钠溶液是过量的,因此又加入了新的杂质.我们自己设计实验方案时,要用适量的稀盐酸溶液.
解答:解:
(1)根据流程图可知:步骤①为溶解,其中玻璃棒搅拌的作用是搅拌,加速溶解;
(2)步骤②、③是固体与液体分离,因此为过滤;
(3)步骤③中,加入过量氢氧化钠溶液的目的是:使镁离子充分与氢氧根反应生成氢氧化镁沉淀,从而使杂质氯化镁完全除去;沉淀B的化学式是Mg(OH)2.
(4)方案步骤③不合理的理由是:加入的氢氧化钠溶液是过量的,则加入了新的杂质.故在除去了氯化钠样品中氯化镁的同时,又引进了氢氧化钠这一新的杂质.
故答案为:
(1)搅拌,加速溶解;
(2)过滤;
(3)使杂质氯化镁完全除去;Mg(OH)2.
(4)由于加入的氢氧化钠溶液是过量的,因此又引入了新的杂质.
(1)根据流程图可知:步骤①为溶解,其中玻璃棒搅拌的作用是搅拌,加速溶解;
(2)步骤②、③是固体与液体分离,因此为过滤;
(3)步骤③中,加入过量氢氧化钠溶液的目的是:使镁离子充分与氢氧根反应生成氢氧化镁沉淀,从而使杂质氯化镁完全除去;沉淀B的化学式是Mg(OH)2.
(4)方案步骤③不合理的理由是:加入的氢氧化钠溶液是过量的,则加入了新的杂质.故在除去了氯化钠样品中氯化镁的同时,又引进了氢氧化钠这一新的杂质.
故答案为:
(1)搅拌,加速溶解;
(2)过滤;
(3)使杂质氯化镁完全除去;Mg(OH)2.
(4)由于加入的氢氧化钠溶液是过量的,因此又引入了新的杂质.
点评:本考点属于物质的分离和提纯,还考查了混合物的分离方法,是中考的重点也是一个难点.本题利用流程图中的现象和实验方案的设计,考查同学们的判断能力,同学们只要认真分析,根据条件综合把握,问题就会迎刃而解.本考点主要出现在实验题中.

练习册系列答案
相关题目
推理是化学学习中常用的思维方法,下列推理正确的是( )
| A、氧化物中都含有氧元素,所以含氧元素的化合物一定是氧化物 |
| B、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
| C、碱的溶液PH大于7,所以PH大于7的溶液一定是碱的溶液 |
| D、化合物都是由不同种元素组成的,所以不同种元素组成的纯净物一定是化合物 |
下列关于水的认识正确的是( )
| A、电解水生成氢气和氧气,则水是由氢气和氧气组成的 |
| B、地球上水量很大,所以淡水资源也很充裕 |
| C、凡澄清、无色透明的液体一定是纯水 |
| D、水被污染后,会给人类造成灾难 |
镁在空气中燃烧的文字表达式是( )
A、镁+氧气
| ||
B、镁条+氧气
| ||
C、镁+空气
| ||
D、镁+氧气
|