题目内容
【题目】填空;
(1)下列燃料中,不属于化石燃料的是__________。(填字母符号)
A 煤 B 石油 C 乙醇 D 天然气
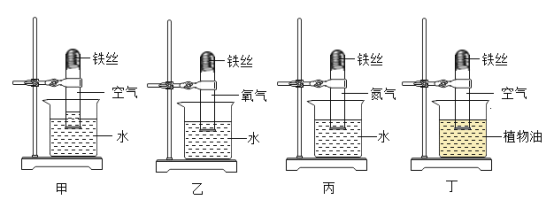
(2)下列防锈措施不合理的是________。(填字母符号)
A 擦去铝锅表面氧化膜
B 在铁制品表面涂油
C 钢管存放在干燥的地方
D 在铁管表面镀上一层不易腐蚀的金属
(3)硝酸钠中的阴离子:_________。(填离子符号)
(4)过氧化钠(Na2O2)与水反应的方程式为:![]() ,则X的化学式为______________。
,则X的化学式为______________。
【答案】C A ![]() O2
O2
【解析】
(1)属于化石燃料的是煤、石油、天然气,乙醇不是化石燃料,故填:C。
(2)A 铝锅表面氧化膜可隔绝空气和水,擦去铝锅表面氧化膜,会使铝锅被腐蚀,不合理;
B 在铁制品表面涂油可隔绝空气和水,保护铁制品,合理;
C 钢管存放在干燥的地方,防止与水接触,可保护钢管,合理;
D 在铁管表面镀上一层不易腐蚀的金属,可保护铁管,合理;
故填:A。
(3)硝酸钠中的阴离子是硝酸根,符号为![]() .。
.。
(4)根据过氧化钠与水反应的方程式为![]() ,由质量守恒定律,X含有两个氧原子,则X的化学式为
,由质量守恒定律,X含有两个氧原子,则X的化学式为![]() 。
。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数。将盛有一定量该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品完全反应,已知烧杯的质量为60.0g,实验过程中的有关数据如下表:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯与所盛物质质量/g | 186.0 | 183.0 | 181.0 | 180.0 | 179.4 | 179.4 |
试计算:
(1)碳酸钙中碳元素与氧元素的质量比(最简比)为_________。
(2)生成二氧化碳的质量为_________g。
(3)求该大理石中碳酸钙的质量分数___________(精确到0.1%)。
【题目】铜元素广泛存在于各种物质中,如CuFeS2、Cu2(OH)2CO3、Cu-Zn合金等。
(1)金属Cu的用途________。(写一条)
(2)写出CuFeS2中Cu的质量分数计算式_________(无需化简)。
(3)现要测定某Cu-Zn合金中Cu的质量。称取l3g该合金粉末于烧杯中,将稀HCl分三次倒入,实验数据如下表所示。
实验编号 | 第一次 | 第二次 | 第三次 |
加入的稀HCl的质量/g | 100 | 100 | 100 |
生成氢气的质量/g | 0.08 | 0.16 | 0.16 |
①分析上表,恰好完全反应的是第__________次实验。
②计算:该l3g合金中Cu的质量______。(根据化学方程式写出完整的计算步骤)。
【题目】某兴趣小组的同学对CO2能否与水反应产生疑问,于是他们从家里找来软塑料瓶进行探究活动,请你参与:
(提出问题)CO2能与水反应吗?
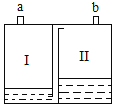
(实验)甲同学按如图所示的实验,打开软塑料瓶塞,迅速将烧杯中的蒸馏水倒入瓶中并拧紧瓶塞,振荡,一会后发现________。
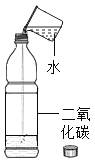
得出结论:CO2能与水反应。
(反思1)乙认为甲的实验不足以证明CO2能与水反应,乙的理由是:______。
(补充实验)取少量甲实验后软塑料瓶中的液体于试管中,向其中滴加紫色石蕊试液,液体变红,乙同学认为这可以说明CO2能与水反应(提示:石蕊是一种遇酸变红的紫色试剂)。
你认为乙同学验证CO2能与水反应的方法,是通过证明______来实现的。
(反思2)丙同学认为乙同学的实验也不足以证明CO2能与水反应,其理由是______。
(再实验)该兴趣小组的同学经过思考、讨论,他们利用蒸馏水、二氧化碳气体和用石蕊试液染成紫色的干燥小花设计了如下实验。请你完成下列实验报告。
实验操作 | 实验现象 | 实验结论 |
(1)______; | 小花仍为紫色 | 水不能使石蕊変色 |
(2)把干燥的紫色小花放入盛有二氧化碳的集气瓶中 | 小花仍为紫色 | ______; |
(3)把实验(1)后的小花放入盛有二氧化碳的集气瓶中 | ______。 | ______。 |
(结论)CO2能与水反应;其化学反应方程式为______。