题目内容
【题目】通过溶解、过滤、蒸发等操作,只能除去粗盐中不溶于水的泥沙等杂质,而粗盐中含有的MgCl2、CaCl2等可溶性杂质无法去除。工业提纯粗盐,得到较纯净精盐的工艺流程如下图所示:

(1)Ca(OH)2溶液的pH________(填“>”“=”或“<”)7;步骤①发生反应的化学方程式为________________________________________________。
(2)步骤③操作a的名称是________。
(3)步骤④加入适量盐酸的目的是除去滤液中的Na2CO3和________;有同学提出:为了确保除去这两种物质,加入过量的稀盐酸也不影响精盐的纯度,理由是____________________________________。
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐中还含有________。
【答案】 > MgCl2+Ca(OH)2===CaCl2+Mg(OH)2↓ 过滤 NaOH 盐酸是氯化氢气体的水溶液,过量的盐酸在蒸发时溶质氯化氢气体挥发,所以不影响精盐的纯度 CaCl2
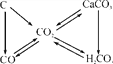
【解析】(1) ![]() 属于常见的碱,PH>7,根据
属于常见的碱,PH>7,根据![]() 与
与![]() 反应原理进行分析;
反应原理进行分析;
(2)根据过滤是分离固液混合物的操作,盐酸在反应中的作用来解答;
(3)根据盐酸的化学性质和蒸发时溶质氯化氢气体挥发进行分析;
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有(1)中加入的过量的氢氧化钙未被除去;
解:(1)氢氧化钙溶液和氯化镁反应生成氢氧化镁沉淀和氯化钙;碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与过量的氢氧化钙反应生成碳酸钙沉淀和![]() ;故填:
;故填:![]() ↓
↓![]() ;
;
(2)步骤(3)是过滤把沉淀氢氧化镁和碳酸钙沉淀过滤分离;
(3)步骤(4)加入适量盐酸的目的是除去滤液中的![]() 和
和![]() ;盐酸是氯化氢气体的水溶液,过量的盐酸在蒸发时溶质氯化氢气体挥发,所以不影响精盐的纯度。故填:过滤,
;盐酸是氯化氢气体的水溶液,过量的盐酸在蒸发时溶质氯化氢气体挥发,所以不影响精盐的纯度。故填:过滤, ![]() ;盐酸是氯化氢气体的水溶液,过量的盐酸在蒸发时溶质氯化氢气体挥发,所以不影响精盐的纯度。
;盐酸是氯化氢气体的水溶液,过量的盐酸在蒸发时溶质氯化氢气体挥发,所以不影响精盐的纯度。
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有过量的氢氧化钙与盐酸反应后的产物![]() 。故填:
。故填: ![]() 。
。

【题目】小亮在实验室发现一瓶盛有无色溶液的试剂,其标签破损,从残余部分只能看出溶质质量分数为10%。具体是什么物质无法辨认。老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种。
(1)小亮查阅氢氧化钙常温下的溶解度为0.18 g后,认为该溶液不可能是氢氧化钙,理由是______________。
(2)小亮取少量样品于试管中,滴加________试液,试液变红色,该溶液不可能是________(填化学式),理由是________________________________________。
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告。
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分。
【进行实验】请你选择一种方案进行实验。
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加该物质 | _____________ | 该溶液是碳酸钠溶液。有关反应的化学方程式为:____________ |
【注意:若答对第(4)小题奖励4分,化学试卷总分不超过60分】
(4)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,该物质可以为________________。
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加该物质 | ________________ | 该溶液是碳酸钠溶液。有关反应的化学方程式为:____________ |