题目内容
【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)

【猜想与假设】
影响过氧化氢分解速率的因素可能有温度、
溶液的浓度、催化剂种类。
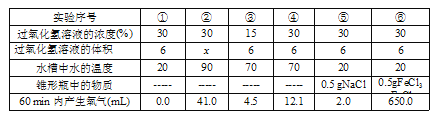
【实验记录】同学们进行6组实验,实验记录如下:
【解释与结论】
(1)实验②中应加入过氧化氢溶液的体积x是______mL。
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定______来比较过氧化氢的分解速率。
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是_____(填序号)。
(4)通过实验①、②、④可得出的结论是______。
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是______(答两点)。
【答案】 6 产生相同体积的氧气所需的时间 ③④ 温度越高,过氧化氢分解速率越大 相同时间内实验②产生氧气少;需要加热;水蒸气含量高
【解析】(1). 实验②中目的是与实验①对照,探究温度对反应速率的影响,应加入过氧化氢溶液的体积x是6mL; (2). 以通过测定产生相同体积的氧气所需的时间来比较过氧化氢的分解速率,需要时间越少,反应速率越快; (3). 得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是③④,因③④只有过氧化氢溶液的浓度不同,可以形成对照实验; (4). 通过实验①、②、④可得出的结论是:温度越高,过氧化氢分解速率越大; (5). 实验室制氧气,应选择实验⑥而不选实验②的理由是:相同时间内实验②产生氧气少;需要加热;水蒸气含量高。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧化钠溶液的反应进行了探究,请你参与并填写以下空白。
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应。
第一组同学设计了实验方案一:
实验步骤 | 实验现象 | 结论 |
先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液,并不断振荡,同时测定混合液的pH | pH逐渐________(填“变大”或“变小”),最后pH≥7 | 稀盐酸与氢氧化钠溶液发生了反应 |
①请你分析:上述方案中为什么强调只有测得的pH≥7才能证明反应了?_____________________________________________。
②写出稀盐酸与氢氧化钠溶液反应的化学方程式________________________________。
(2)第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后,为探究稀盐酸与氢氧化钠溶液是否恰好完全反应,设计了实验方案二:
实验步骤 | 实验现象 | 结论 |
取少量上述反应后的溶液于试管中,滴加酚酞溶液 | 若______________ | 氢氧化钠溶液过量 |
若无明显现象 | 稀盐酸与氢氧化钠溶液恰好完全反应 |
此时有同学提出方案二不能证明稀盐酸与氢氧化钠溶液恰好完全反应,其原因是________________________________,为此,还需要选择________________或________,再进行实验即可。
【题目】在一个密闭容器中有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,可判断该容器中发生化学反应的基本类型为( )
物质 | A | B | C | D |
反应前质量/g | 2 | 2 | 32 | 5 |
反应后质量/g | 待定 | 20 | 0 | 12 |
A.C=A+B+D B.B+C+D=A C.A=B+C+D D.B+D=A+C