题目内容
为了测定铜锌合金的组成,某化学课外活动小组利用取了10克合金与稀盐酸反应,最后收集到氢气的质量是0.2克,求:
(1)求合金中锌的质量;
(2)求合金中锌的质量分数.
(1)求合金中锌的质量;
(2)求合金中锌的质量分数.
分析:(1)根据生成的氢气的质量结合反应的化学方程式可以求出合金中锌的质量;
(2)根据求出的锌的质量可以求出合金中锌的质量分数.
(2)根据求出的锌的质量可以求出合金中锌的质量分数.
解答:解:(1)设合金中锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
=
解得x=6.5g,
(2)合金中锌的质量分数为:
×100%=65%
答:(1)求合金中锌的质量为6.5g;
(2)合金中锌的质量分数65%.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| x |
| 2 |
| 0.2g |
解得x=6.5g,
(2)合金中锌的质量分数为:
| 6.5g |
| 10g |
答:(1)求合金中锌的质量为6.5g;
(2)合金中锌的质量分数65%.
点评:本题主要考查学生根据化学方程式进行计算的能力,明确生成氢气的质量和对应的化学反应的关系是解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(2010?南开区一模)黄铜是由锌和铜形成的合金(合金可视为均一的混合物)有较强的耐磨性能,在生活中有广泛的用途.晓军同学为了测定黄铜屑样品的组成,分四次取样品与稀硫酸反应,其实验数据记录如下,其中过量的黄铜屑样品与稀硫酸反应的数据组是( )
|
为了测定某铜锌合金中铜的质量分数,某实验小组的同学做了以下两组实验探究:
(1)第一组同学设计了如下实验:
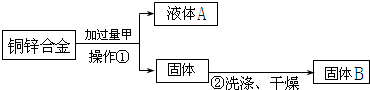
他们认为做完以上操作后,再称量所得固体B的质量,即可求出合金中铜的质量分数,从上述流程图中可以看出,操作①为________,甲物质可以是________,固体B为________,小刚发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是________.
(2)第二组同学利用该合金与稀硫酸反应,根据生成氢气的质量先求出锌的质量,从而解决了问题.他们共进行了三次实验,所得的相关实验数据记录如下(不计实验中产生的误差):
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 20 | 20 | 40 |
| 所用的稀硫酸的质量/g | 100 | 120 | 80 |
| 生成的氢气的质量/g | 0.4 | 0.4 | 0.4 |
(1)当所取合金与所用稀硫酸的质量比为________时,合金中的锌与稀硫酸恰好完全反应.
(2)求该合金中铜的质量分数.(写出计算过程)
为了测定某铜锌合金中铜的质量分数,某实验小组的同学做了以下两组实验探究:
(1)第一组同学设计了如下实验:
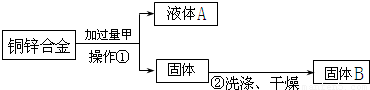
他们认为做完以上操作后,再称量所得固体B的质量,即可求出合金中铜的质量分数,从上述流程图中可以看出,操作①为______,甲物质可以是______,固体B为______,小刚发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是______.
(2)第二组同学利用该合金与稀硫酸反应,根据生成氢气的质量先求出锌的质量,从而解决了问题.他们共进行了三次实验,所得的相关实验数据记录如下(不计实验中产生的误差):
从上表数据分析,
(1)当所取合金与所用稀硫酸的质量比为______时,合金中的锌与稀硫酸恰好完全反应.
(2)求该合金中铜的质量分数.(写出计算过程)
(1)第一组同学设计了如下实验:

他们认为做完以上操作后,再称量所得固体B的质量,即可求出合金中铜的质量分数,从上述流程图中可以看出,操作①为______,甲物质可以是______,固体B为______,小刚发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是______.
(2)第二组同学利用该合金与稀硫酸反应,根据生成氢气的质量先求出锌的质量,从而解决了问题.他们共进行了三次实验,所得的相关实验数据记录如下(不计实验中产生的误差):
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 20 | 20 | 40 |
| 所用的稀硫酸的质量/g | 100 | 120 | 80 |
| 生成的氢气的质量/g | 0.4 | 0.4 | 0.4 |
(1)当所取合金与所用稀硫酸的质量比为______时,合金中的锌与稀硫酸恰好完全反应.
(2)求该合金中铜的质量分数.(写出计算过程)
黄铜是由锌和铜形成的合金(合金可视为均一的混合物)有较强的耐磨性能,在生活中有广泛的用途.晓军同学为了测定黄铜屑样品的组成,分四次取样品与稀硫酸反应,其实验数据记录如下,其中过量的黄铜屑样品与稀硫酸反应的数据组是( )
A.A
B.B
C.C
D.D
| 备选答案 | 样品质量/g | 稀盐酸的质量/g | 产生气体的质量/g |
| A | 25.0 | 80 | 0.4 |
| B | 25.0 | 100 | 0.5 |
| C | 25.0 | 120 | 0.5 |
| D | 30.0 | 100 | 0.5 |
A.A
B.B
C.C
D.D