题目内容
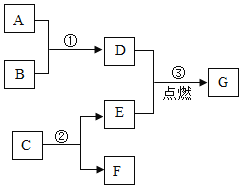
【题目】我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料制取黄铜(铜和锌的合金,外观似黄金),其生产流程如下:

回答下列问题:
(1)木炭需要研成粉状,是为了_____________。
(2)黄铜的硬度比铜和锌都__________(填大小)。
(3)加热时,发生的主要反应化学方程式为:①ZnCO3![]() ZnO+CO2↑;②2ZnO+C
ZnO+CO2↑;②2ZnO+C![]() 2Zn+CO2↑;③______________(赤铜和木炭粉反应)。
2Zn+CO2↑;③______________(赤铜和木炭粉反应)。
(4)气体A中,除CO2外还会含有CO,写出其中产生CO的反应化学方程式________________。
(5)鉴别黄铜和黄金有多种方法,写出一种鉴别方法:__________。
【答案】增大接触面积,使反应更充分彻底 大 2Cu2O+C![]() 4Cu+CO2↑ C+CO2
4Cu+CO2↑ C+CO2![]() 2CO 取少量样品滴加稀硫酸,若有气泡产生,则为黄铜,反之则为黄金(操作+现象+结论,合理即可)
2CO 取少量样品滴加稀硫酸,若有气泡产生,则为黄铜,反之则为黄金(操作+现象+结论,合理即可)
【解析】
(1)研磨的目的是增大反应物接触面积,使反应物充分混合,使反应更彻底;
(2)合金的硬度比组成它的金属的硬度大,黄铜是铜锌合金,故黄铜的硬度比纯铜、纯锌大;
(3)赤铜和木炭粉在800℃时反应生成二氧化碳和铜单质,化学反应方程式为:2Cu2O+C![]() 4Cu+CO2↑;
4Cu+CO2↑;
(4)木炭在高温下和反应生成的二氧化碳反应生成一氧化碳,化学反应方程式为:C+CO2![]() 2CO;
2CO;
(5)黄铜是铜锌合金,锌可以可稀硫酸反应,生成氢气,故取少量样品滴加稀硫酸,若有气泡产生,则为黄铜,反之则为黄金。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 加入足量锌粉 |
B | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
C | 检验蜡烛燃烧的产物中是否有水 | 在火焰上方罩一只冷而干燥的烧杯 |
D | 分离铜粉和铁粉 | 加水,过滤 |
A. A B. B C. C D. D