题目内容
通过本单元学习,你已经掌握了实验室制取气体的有关规律,请你结合如图装置图回答问题:
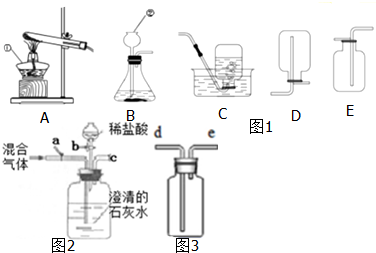
(1)写出图中指定仪器的名称:甲 ,乙 ,丙 .
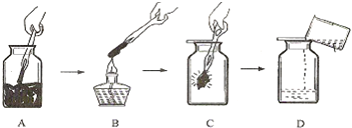
(2)收集CO2应选择 装置,检验CO2收集满瓶的方法是 .
(3)若要检验气体是否为 CO2,应选择装置 ,气体应从 处通入,该装置中观察到的实验现象是
(4)若要证明二氧化碳能与水反应,应选择装置
(5)烧杯H中放有燃着的蜡烛,若将CO2气体从导管通入烧杯中,观察到的实验现象是 (填“上”或“下”)层蜡烛先熄灭,此实验证明CO2有 、 、 的性质.
(6)在通常情况下,硫化氢(H2S)是一种没有颜色的气体,有毒.能溶于水,比空气的密度大.实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,同时又生成硫酸亚铁(FeSO4),根据上图回答下列问题:
①实验室制取H2S气体时,可选用的发生装置是 收集装置是
②实验室制取H2S气体的化学方程式为 .

(1)写出图中指定仪器的名称:甲
(2)收集CO2应选择
(3)若要检验气体是否为 CO2,应选择装置
(4)若要证明二氧化碳能与水反应,应选择装置
(5)烧杯H中放有燃着的蜡烛,若将CO2气体从导管通入烧杯中,观察到的实验现象是
(6)在通常情况下,硫化氢(H2S)是一种没有颜色的气体,有毒.能溶于水,比空气的密度大.实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,同时又生成硫酸亚铁(FeSO4),根据上图回答下列问题:
①实验室制取H2S气体时,可选用的发生装置是
②实验室制取H2S气体的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,二氧化碳的实验室制法,二氧化碳的检验和验满,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从仪器的图形和用途去分析解答;
(2)从二氧化碳气体的密度比空气大、能溶于水,由于二氧化碳的密度比空气大,将燃着的木条放在集气瓶口,如果熄灭,证明已满去分析解答;
(3)从通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,观察到的现象是石灰水变浑浊;由于F装置内有石灰水,所以气体应从a端进入,否则石灰水会被压出去分析解答;
(4)从二氧化碳和不反应生成碳酸,碳酸显酸性,能使紫色石蕊变红(二氧化碳不是酸不能使紫色石蕊变红)去分析解答;
(5)从二氧化碳既不燃烧也不支持燃烧,因此两支蜡烛都会熄灭,由于二氧化碳的密度比空气大,所以下层的蜡烛先熄灭去分析解答;
(6)①从实验室制取H2S气体,是固体和液体反应且不需加热,硫化氢(H2S)能溶于水,比空气的密度大去分析解答;
②从反应物是硫化亚铁固体(FeS)和稀硫酸(H2SO4),生成物是H2S气体和硫酸亚铁,反应条件是常温去分析解答;
(2)从二氧化碳气体的密度比空气大、能溶于水,由于二氧化碳的密度比空气大,将燃着的木条放在集气瓶口,如果熄灭,证明已满去分析解答;
(3)从通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,观察到的现象是石灰水变浑浊;由于F装置内有石灰水,所以气体应从a端进入,否则石灰水会被压出去分析解答;
(4)从二氧化碳和不反应生成碳酸,碳酸显酸性,能使紫色石蕊变红(二氧化碳不是酸不能使紫色石蕊变红)去分析解答;
(5)从二氧化碳既不燃烧也不支持燃烧,因此两支蜡烛都会熄灭,由于二氧化碳的密度比空气大,所以下层的蜡烛先熄灭去分析解答;
(6)①从实验室制取H2S气体,是固体和液体反应且不需加热,硫化氢(H2S)能溶于水,比空气的密度大去分析解答;
②从反应物是硫化亚铁固体(FeS)和稀硫酸(H2SO4),生成物是H2S气体和硫酸亚铁,反应条件是常温去分析解答;
解答:解:(1)由仪器的图形和用途可知:甲为试管,乙为长颈漏斗,丙为集气瓶;故答案为:试管,长颈漏斗,集气瓶;
(2)二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,故收集装置为C;由于二氧化碳的密度比空气大,将燃着的木条放在集气瓶口,如果熄灭,证明已满;故答案为:C 燃着的木条放在集气瓶口,如果熄灭,证明已满;
(3)通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,观察到的现象是石灰水变浑浊;由于F装置内有石灰水,所以气体应从a端进入,否则石灰水会被压出;故答案为:F a 石灰水变浑浊;
(4)二氧化碳和不反应生成碳酸,碳酸显酸性,能使紫色石蕊变红(二氧化碳不是酸不能使紫色石蕊变红),故答案为:G;
(5)由于二氧化碳既不燃烧也不支持燃烧,因此两支蜡烛都会熄灭,由于二氧化碳的密度比空气大,所以下层的蜡烛先熄灭;故答案为:下 既不燃烧 也不支持燃烧 密度比空气大;
(6)①实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,由于是固体和液体反应且不需加热,故发生装置应为B;硫化氢(H2S)能溶于水,所以不能用排水法收集;比空气的密度大,所以可用向上排空气法收集.故答案为:B C;
②实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,同时又生成硫酸亚铁(FeSO4),反应物是硫化亚铁固体(FeS)和稀硫酸(H2SO4),生成物是H2S气体和硫酸亚铁,反应条件是常温,所以反应的化学方程式为:FeS+H2SO4═FeSO4+H2S↑;故答案为:FeS+H2SO4═FeSO4+H2S↑.
(2)二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,故收集装置为C;由于二氧化碳的密度比空气大,将燃着的木条放在集气瓶口,如果熄灭,证明已满;故答案为:C 燃着的木条放在集气瓶口,如果熄灭,证明已满;
(3)通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,观察到的现象是石灰水变浑浊;由于F装置内有石灰水,所以气体应从a端进入,否则石灰水会被压出;故答案为:F a 石灰水变浑浊;
(4)二氧化碳和不反应生成碳酸,碳酸显酸性,能使紫色石蕊变红(二氧化碳不是酸不能使紫色石蕊变红),故答案为:G;
(5)由于二氧化碳既不燃烧也不支持燃烧,因此两支蜡烛都会熄灭,由于二氧化碳的密度比空气大,所以下层的蜡烛先熄灭;故答案为:下 既不燃烧 也不支持燃烧 密度比空气大;
(6)①实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,由于是固体和液体反应且不需加热,故发生装置应为B;硫化氢(H2S)能溶于水,所以不能用排水法收集;比空气的密度大,所以可用向上排空气法收集.故答案为:B C;
②实验室用块状硫化亚铁固体(FeS)和稀硫酸(H2SO4)(液体)常温反应来制取H2S气体,同时又生成硫酸亚铁(FeSO4),反应物是硫化亚铁固体(FeS)和稀硫酸(H2SO4),生成物是H2S气体和硫酸亚铁,反应条件是常温,所以反应的化学方程式为:FeS+H2SO4═FeSO4+H2S↑;故答案为:FeS+H2SO4═FeSO4+H2S↑.
点评:实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ”和“
”和“ ”分别表示质子数不同的两种原子,则下列图中表示化合物的是
”分别表示质子数不同的两种原子,则下列图中表示化合物的是

 、
、 、
、 ”分别表示A,B、C三种不同的分子,其在一定条件下反应前后的变化 请回答
”分别表示A,B、C三种不同的分子,其在一定条件下反应前后的变化 请回答