题目内容
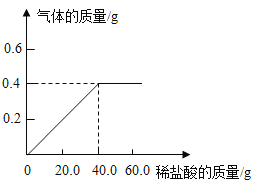
【题目】铜锌合金又称假黄金。向盛有20g铜锌合金粉末样品的烧杯中逐渐加入稀盐酸,生成氢气的质量与加入稀盐酸的质量关系如图所示,请计算:
(1)合金样品中铜的质量分数_________。
(2)恰好完全反应时,所得溶液中溶质的质量分数________。(结果精确到0.1%)
【答案】35% 51.7%
【解析】
根据图可以知道生成氢气的质量为0.4g,根据氢气的质量和对应的化学方程式求算锌的质量和氯化锌的质量,进而求算对应的质量分数。
(1)解:根据图可知生成的氢气的质量为0.4g。
设合金样品中锌的质量为x,充分反应后生成氯化锌的质量为y
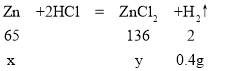
![]()
解得:x=13g y=27.2g
合金样品中铜的质量分数是:![]() =35%。
=35%。
答:合金样品中铜的质量分数为35%。
(2)恰好完全反应时,所得溶液中溶质的质量分数是:![]() ≈51.7%
≈51.7%
答:恰好完全反应时所得溶液溶质的质量分数为51.7%。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目