题目内容
【题目】草酸存在于自然界的植物中。草酸晶体(H2C2O42H2O)无色固体,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。草酸能与氢氧化钙反应生成沉淀。请完成下列实验:
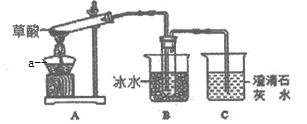
实验一、甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置B的主要作用是_____。装置C中有气泡逸出,澄清石灰水变浑浊,由此可知草酸晶体分解的产物中一定有_____。
实验二、乙组同学认为草酸晶体分解的产物中还有CO,为进行验证,兴趣小组同学设计了如图装置:
(信息提供)
①氢氧化钠溶液能很好的吸收二氧化碳。
②浓硫酸是实验室里一种常用的干燥剂,能干燥某些气体。
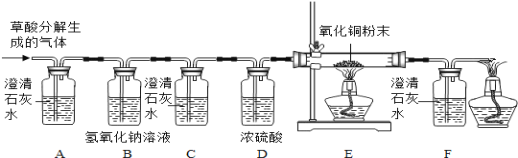
(探究)
(1)实验过程中观察到A装置中澄清石灰水变浑浊,证明有CO2气体,写出A中发生反应的方程式_____;
(2)实验过程中还观察到以下现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③_____,证明有CO气体。
(结论)通过上述探究:草酸晶体分解的化学方程式是_____。
(讨论)装置末端酒精灯的作用是_____。
(定量探究)
某同学在实验结束后,收集装置F中的白色固体,测其质量为5g,则参加反应的一氧化碳的质量是多少?(写出计算过程)_____。
【答案】冷却草酸蒸气,防止与澄清石灰水反应生成白色沉淀,干扰二氧化碳的检验 二氧化碳 CO2+Ca(OH)2=CaCO3↓+H2O F装置中澄清石灰水变浑浊 H2C2O4 CO2↑+CO↑+H2O 处理尾气CO,防止污染空气 1.4g
CO2↑+CO↑+H2O 处理尾气CO,防止污染空气 1.4g
【解析】
实验一、草酸能与氢氧化钙反应生成沉淀,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以装置B的主要作用是:冷却草酸蒸气,防止与澄清石灰水反应生成白色沉淀,干扰二氧化碳的检验;装置C中有气泡逸出,澄清石灰水变浑浊,由此可知草酸晶体分解的产物中一定有:二氧化碳;
实验二、[探究] (1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)实验过程中还观察到以下现象:①C装置中澄清石灰水不变浑浊(说明通入的气体中不含二氧化碳);②E装置中黑色粉末变成红色(说明黑色的氧化铜被还原,生成铜);③_____,若要证明通入的气体中含有CO气体,则只需证明有二氧化碳气体生成即可,故现象③为F装置中澄清石灰水变浑浊;
[结论]根据实验现象可知,生成物中一定有一氧化碳、二氧化碳和水,故草酸晶体分解的化学方程式是:H2C2O4 CO2↑+CO↑+H2O;
CO2↑+CO↑+H2O;
[讨论]为防止一氧化碳污染空气,装置末端的酒精灯可以点燃尾气一氧化碳,防止污染空气。故填:处理尾气CO,防止污染空气;
[定量探究]设参加反应的一氧化碳的质量为x。由CO+CuO![]() Cu+CO2、CO2+Ca(OH)2=CaCO3↓+H2O可知:
Cu+CO2、CO2+Ca(OH)2=CaCO3↓+H2O可知:
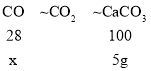
![]()
x=1.4g
答:参加反应的一氧化碳的质量是1.4g。

 亮点激活精编提优100分大试卷系列答案
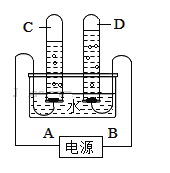
亮点激活精编提优100分大试卷系列答案【题目】通常条件下水的沸点是100℃,随着压强增大,水的沸点会逐渐升高。如图是研究水沸点随气压变化的实验。关闭止水夹,连接好装置, 再将液体 A滴入试管②中,打开夹子,试管①内的水立刻沸腾。则液体A和气体B的组合可能是
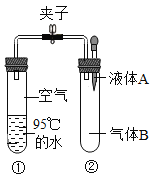
序号 | A | B | C | D |
液体A | 水 | 水 | 石灰水 | 水 |
气体B | 氮气 | 氧气 | 二氧化碳 | 氢气 |
A.AB.BC.CD.D
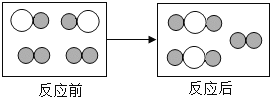
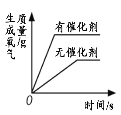
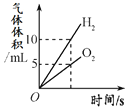
【题目】下列图像能正确反映对应变化关系的是
|
|
|
|
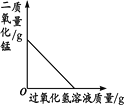
A.用等质量、等浓度的双氧水制取氧气 | B.利用红磷燃烧测定空气中氧气的含量(打开止水夹前) | C.将水通电电解一段时间 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D