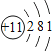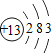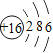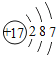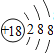题目内容
【题目】元素周期表是学习和研究化学的重要工具。下表是1—3周期元素的部分信息,请认真分析表中信息,回答下列问题。
| IA | 0 | ||||||
1 |
| IIA | IIIA | IVA | VA | VIA | VIIA |
|
2 |
|
|
|
|
|
|
|
|
3 |
|
|
| Z |
|
|
|
|
(1)相对原子质量为20.18的元素,其原子序数为_____,核电荷数为7的元素属于__________(填“金属元素”或“非金属元素”)。
(2)第二周期共有______种元素,该周期元素原子的质子数从左到右依次_________(填“递增” 或“递减”)。
(3)3号元素和11号元素的化学性质相似的,原因是它们的__________数相同;周期表中Z元素的原子最外层电子数为____________
【答案】10 非金属元素 8 递增 最外层电子 4
【解析】
(1)相对原子质量在元素符号的正下方,20.08在氖元素正下方,根据表中信息可以得出,此元素为氖,因此其原子序数为10;核电荷数与原子序数相等,所以核电荷数为7的元素,其原子序数也为7,从表中可以看出为氮元素,属于非金属元素;
故答案为:10;非金属元素。
(2)从第二周期可以看出,一共有锂、铍、硼、碳、氮、氧、氟和氖等8种元素;质子数与原子序数相等,从左到右原子序数依次递增,因此质子数也是依次递增;
故答案为:8;递增。
(3)化学性质是由最外层电子数决定,3号元素和11号元素的化学性质相似,说明它们的最外层电子数相同;Z为14号元素,其外部电子排布为2、8、4,所以最外层电子数为4;
故答案为:最外层电子;4

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案【题目】下列图像能正确反映对应的变化关系的是
|
|
|
|
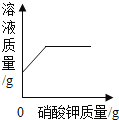
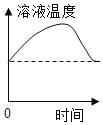
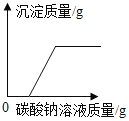
A.常温下,向一定量的水中加入硝酸钾晶体 | B.硝酸铵溶于水时溶液的温度变化 | C.向稀盐酸和氯化钡的混合溶液中加入碳酸钠溶液 | D.CO 和过量的氧气在密闭容器中完全反应 |
A.AB.BC.CD.D
【题目】某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,实验数据如下表,请认真分析数据,回答下列问题。
甲 | 乙 | 丙 | |
烧杯+稀硫酸 | 150g | 100g | 100g |
加入的铁样品 | 6g | 6g | 10g |
充分反应后,烧杯+剩余物 | 155.8g | 105.8g | 109.8g |
(1)三位同学中_____(填甲、乙或丙)所取的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;_____
(3)计算恰好完全反应后所得溶液中溶质的质量分数_______。(烧杯的质量为25.48g)