题目内容
【题目】化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为A、B、C并设计了如图实验方案。
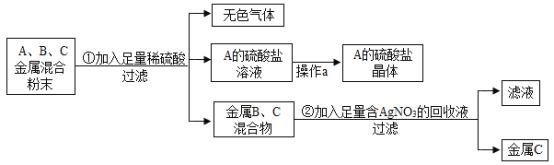
(1)A、B、C三种金属的活动性顺序为_____。
(2)已知A的硫酸盐中A元素显+2价,请写出①中发生反应的化学方程式_____。
(3)判断②中过滤后所得的滤液中AgNO3是否有剩余,可加入_____确定。
【答案】A>B>C ![]() 稀盐酸等
稀盐酸等
【解析】
(1)由图可知,A能与硫酸反应,而B、C不能与硫酸反应,说明A的活动性比B、C的强;将B、C金属混合物加入足量的硝酸银溶液中,B反应,C没有反应,说明B的活动性比C的强,三种金属的活动性顺序为A>B>C;
(2)铜、锰、银三种金属中,锰在金属活动性顺序表中排在氢前,能与稀硫酸反应,所以A为锰,已知A的硫酸盐中A元素显+2价,①中发生反应的化学方程式![]() ;
;
(3)硝酸银溶液能与稀盐酸(或氯化钠溶液等)生成氯化银白色沉淀,判断②中过滤后所得的滤液中AgNO3是否有剩余,可通过加入与稀盐酸(或氯化钠溶液等),如果生成白色沉淀,则有硝酸银,反之,则没有。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实验装置 |
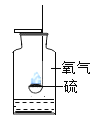
硫在氧气中燃烧 |
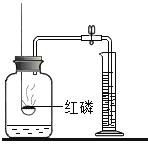
测定空气中氧气含量 |
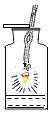
铁丝在氧气中燃烧 |
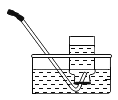
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热 | 量简中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:先将集气瓶内的空气排净,后便于观察H2何时收集满 |
A.AB.BC.CD.D
【题目】将一定量的乙醇(C2H5OH)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X.测得反应前后物质的质量如表.下列判断正确的是( )
物 质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
A.表中m的值为2.8
B.X可能是该反应的催化剂
C.该反应分解反应
D.物质X一定含有碳元素,可能含有氢元素