题目内容
【题目】将等质量、颗粒大小相同的X、Y、Z三种金属分别投入到相同浓度的足量的稀硫酸中,生成氢气的质量与时间的关系如图所示。已知它们在化合物中均显+2价,则下列说法不正确的是( )
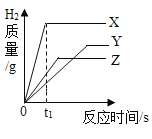
A.在时间为t1时,生成氢气的质量为:X>Z>Y
B.金属活动性:X>Z>Y
C.相对原子质量:X>Y>Z
D.X、Y和Z可能分别是常见金属中的Mg、Fe、Zn
【答案】C
【解析】
试题A、根据图示,在时间为t1时,生成氢气的质量为:X>Z>Y,正确,B、根据反应所需时间越短,说明反应速率越快,金属活动性越强,故金属活动性:X>Z>Y[,正确,C、当金属质量相等,且均形成+2价的化合物,那么生成的氢气质量与金属的相对原子质量成反比,即金属的相对原子质量越大,生成的氢气质量就越小,故根据生成氢气质量关系X>Y>Z,则相对原子质量:Z>Y>X,错误,D、根据上面的分析,金属活动性:X>Z>Y[,相对原子质量:Z>Y>X,故X、Y和Z可能分别是常见金属中的Mg、Fe、Zn,正确,故选C

 考前必练系列答案
考前必练系列答案【题目】20℃时,向下列3只盛有100g水的烧杯中,分别加入40g三种固体,充分溶解。
温度/℃ | NaCl | KNO3 | NaNO3 |
20 | 36.0g | 31.6g | 88g |
60 | 37.3g | 110g | 125g |
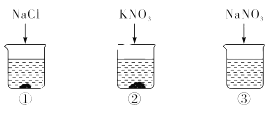
将三份溶液升温至60℃,下列说法正确的是()
A.①②③的溶质质量分数都发生改变
B.①②③都变成不饱和溶液
C.②中溶质和溶剂的质量比为2:5
D.溶液质量②<③
【题目】化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图一所示),于是他们对这个异常现象进行了探究.
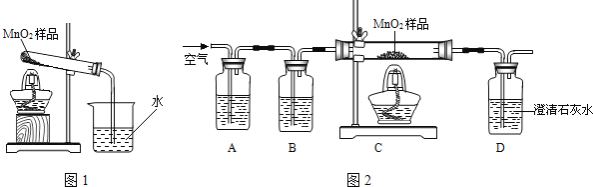
(1)对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭.将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是 .
(2)对气体来源的探究:
甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
实验步骤及现象 | 结论 |
加热空的试管,另一端的澄清石灰水没有变浑浊 | 假设 (填“不成立”或“成立”). |
乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体.他设计了如图二所示的实验进行研究,其中B装置的作用是检验A中反应是否完全,B中的试剂是 ,实验中观察到D处澄清石灰水变浑浊.他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊.
通过乙同学的实验证明,二氧化锰中混有炭粉,炭粉与 反应产生了这种气体.
【题目】理科实验操作考试中,小明同学在做铝和稀盐酸反应时无意中加入几滴硫酸铜溶液,发现铝片表面产生气泡速率明显增快,对此他产生了兴趣。
(提出问题)硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
(设计并实验)室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10%稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率。
实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
饱和硫酸铜溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(1)如表表格中V=____________;
(2)写出铝和稀盐酸反应的化学方程式____________:
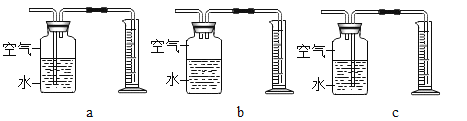
(3)定量收集氢气体积可用如图____________(填写字母序号)装置。
(实验现象)随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表面附着的红色物质逐渐增加。
(结论与解释)
(4)随着硫酸铜体积的增加,反应速率明显变慢可能的原因是____________;
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是____________;
(实验反思)加速铝和稀硫酸反应速率还可以采取的措施是(写出一点)____________
(若正确回答下列小题奖励4分,化学试卷不超过60分)
(实验拓展)根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10%稀盐酸混合后加入不同的盐溶液,实验现象如表(加号越多,代表反应速率越快):
实验1 | 实验2 | 实验3 | 实验4 | 实验5 | |
加入试剂0.5mL | 水 | 5%NaCl溶液 | 5%Mg(NO3)2溶液 | 5%FeSO4溶液 | 5%CuSO4溶液 |
产生气泡速率 | + | + | + | ++ | +++ |
(6)如表中,用水进行实验的目的___;
(7)上述实验设计存有缺陷,该缺陷是___;实验改进后,任符合上表中的实验现象,可得到的实验结论是:①____________;②____________.
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |